由新冠病毒(SARS-CoV-2)引起的新冠肺炎(COVID-19)已在全球迅速蔓延,世界正承受著相當大的健康、社會和經濟負擔。因此,快速準確地識別和監測SARS-CoV-2感染對于預防疾病傳播和最終挽救生命至關重要。由于具有同時切割靶向核酸和非靶向核酸(用作報告分子)并輸出信號的特性,CRISPR-Cas系統近期開始被應用在核酸檢測中,在新型生物傳感器構建中表現出了巨大的潛力。同時,電化學分析方法具有的高靈敏度、快速響應和成本效益優勢使電化學生物傳感器成為醫學診斷中強大的分析工具。
據麥姆斯咨詢報道,近期,深圳大學光電工程學院研究人員于Nano-Micro Letters期刊發表題為“CRISPR-Cas12a-Empowered Electrochemical Biosensor for Rapid and Ultrasensitive Detection of SARS-CoV-2 Delta Variant”的研究論文。該研究開發了一種基于CRISPR-Cas系統的新型電化學生物傳感器,用于檢測SARS-CoV-2德爾塔(Delta)變異株。
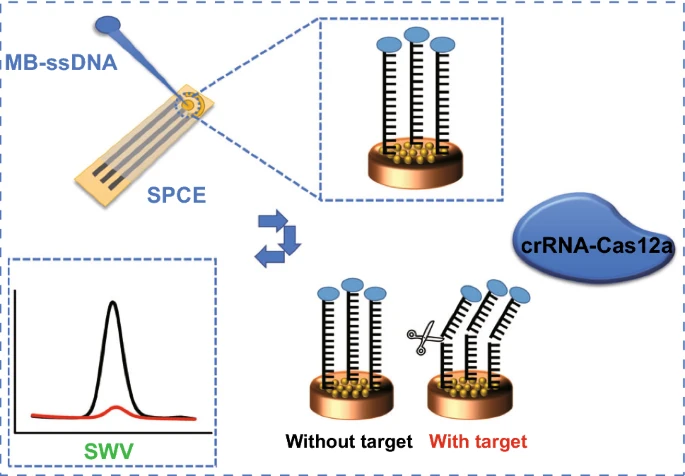
為了增強傳感性能,工作電極(AuE)使用電沉積高質量金納米顆粒修飾得到AuE-AuNPs,以增加導電性和活性比表面積。然后用亞甲藍單鏈DNA(MB-ssDNA)修飾AuE-AuNPs。為了穩定的電化學信號和長時間存儲,選擇了Cas12a蛋白來制造生物傳感器。當生物傳感器被Cas12a-crRNA-靶標DNA混合溶液處理時,在特異性識別靶標DNA的作用下,Cas12a的反式切割活性激活,MB-ssDNA將從電極表面被切割。因此,AuE-AuNPs和ssDNA上的氧化還原介體(MB)之間的電子轉移在切割前后發生了變化,而這種變化可以通過電化學轉導和檢測。研究分別通過生物學和電化學策略檢驗了該傳感器的可行性,并繼續傳感器的檢測限(LOD)、特異性、穩定性以及在即時檢測(POCT)中的性能和應用潛力。
金納米顆粒輔助CRISPR電化學生物傳感器的原理
首先將MB-ssDNA報告基因固定于修飾電極表面。基于靶標的前間區序列鄰近基序(PAM)以及靶DNA與crRNA的互補性,設計了導向Cas12a/crRNA雙鏈體,以特異性識別SARS-COV-2的靶標DNA。在沒有目標DNA的情況下,Cas12a-crRNA的切割活性未被激活,MB-ssDNA報告分子保留在修飾電極表面,從而產生了明顯的MB電化學信號。在靶標DNA存在的情況下,Cas蛋白識別PAM序列,Cas12a的反式切割活性被激活,因此MB-ssDNA報告基因被從電極表面非特異性切割,導致MB的電化學信號降低。得益于金納米顆粒的大比表面積,可以將目標識別事件轉化為電極上ssDNA報告基因的大量切割,用于設計高靈敏度的電化學核酸生物傳感器。
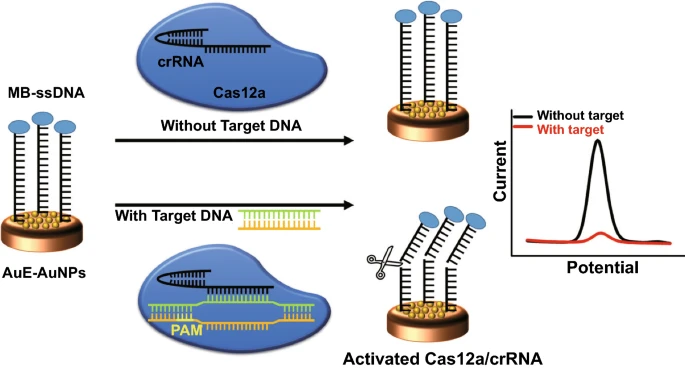
圖1 金納米顆粒輔助CRISPR電化學生物傳感器的原理示意圖。CRISPR電化學生物傳感器的生物可行性探究為了檢驗基于CRISPR-Cas12a的電化學生物傳感器用于核酸檢測的可行性,在設備上檢測之前進行了驗證實驗。如圖2A所示,設計了不同的目標模板并將其插入pUC57質粒中。使用瓊脂糖凝膠電泳確認順式和反式切割。如圖2B所示,觀察到完整dsDNA模板的條帶(表示為“T”)。在圖2C中,只有Delta變體的DNA模板與CRISPR系統發生反應并觀察到強熒光。此外,FAM-ssDNA-BHQ探針被用作Cas12a的報告基因,用于熒光檢測具有不同濃度(從100fM到10nM)的目標Delta DNA,計算檢測下限約為100pM(圖 2D)。
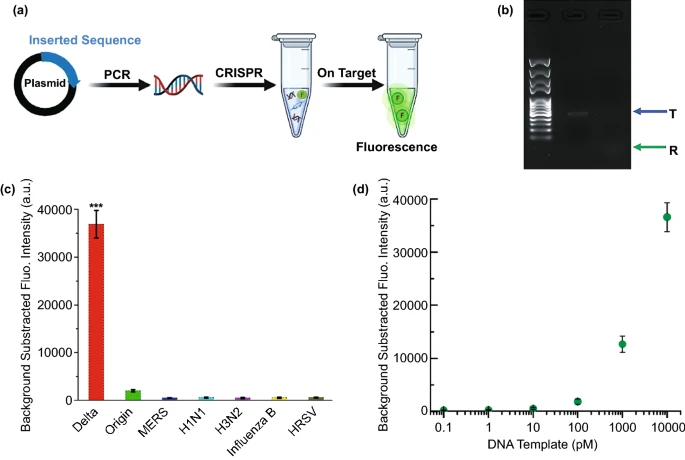
圖2 (A)CRISPR反應示意圖;(B)通過瓊脂糖凝膠電泳驗證反式和順式切割;(C)crRNA的特異性;(D)熒光濃度結果,灰線表示檢測限。CRISPR電化學生物傳感器的電化學可行性探究首先對生物傳感器不同階段的電化學阻抗譜(EIS)進行了驗證,如圖3A所示,AuE-AuNPs具有優異的電化學電導率(黑色曲線)。在將MB-ssDNA固定在AuE-AuNPs上后,Ret值顯著增加至4795Ω(紅色曲線),在用Cas12a-crRNA-靶DNA混合溶液處理后,由于Cas12a的活化切割活性,大部分MB-ssDNA已被切割并與AuE-AuNPs分離導致Ret在藍色曲線中大幅下降(約1612Ω)。SWV如圖3B所示,當生物傳感器用Cas12a-crRNA混合溶液處理沒有靶DNA時,在-0.27有明顯的MB的氧化還原峰(黑色曲線);當生物傳感器用Cas12a-crRNA與靶DNA一起處理時,MB的氧化還原峰顯著降低(紅色曲線),這進一步證實了MB-ssDNA的成功切割和MB在生物傳感器表面的釋放。圖3C顯示了MB的氧化還原峰的SWV,靶DNA濃度范圍為100fM至10nM,其中隨著靶DNA濃度的增加,電流逐漸減小。在圖4中,電流變化(ΔI%)與目標 DNA濃度的對數得到的回歸方程為:ΔI% = 14.37lgC + 192.67,R2和LOD分別計算為0.987和50fM。
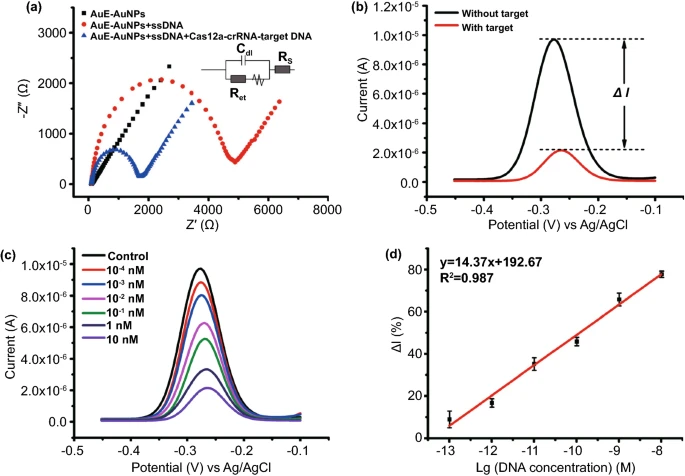
圖3 (A)電化學阻抗譜(EIS)表征;(B)方波伏安(SWV)曲線;(C)不同濃度靶DNA的SWV曲線;(D)電流變化(ΔI%)與目標DNA濃度的對數之間的線性關系。
CRISPR電化學生物傳感器的特異性探究
如圖4所示,當靶標DNA被來自原始SARS-CoV-2病毒的核酸取代時,觀察到明顯降低的ΔI%(16.1%),這證實了crRNA靶向Delta變體的特異性。此外,MERS、H?N?、H?N?、B型流感和HRSV均表現出不明顯的信號變化(ΔI% < 10%),而僅來自Delta變體的靶標DNA表現出顯著的電化學響應(ΔI% = 77.9%)。該實驗結果表明建立的電化學生物傳感器能夠以高特異性檢測SARS-COV-2 Delta變體。
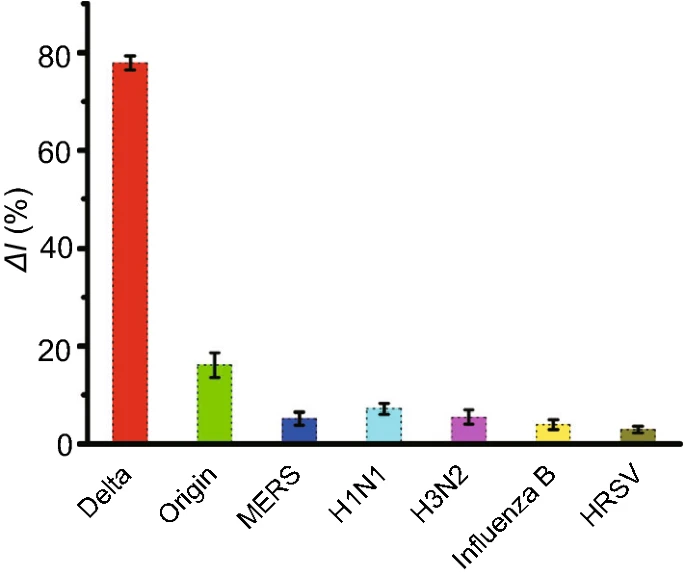
圖4 AuNPs輔助E-CRISPR對SARS-COV-2 Delta變體的特異性分析。根據SWV電流計算信號變化,分別添加目標DNA(10nM)和非目標病毒(10nM)。
CRISPR電化學生物傳感器的即時檢測應用探究
微型電化學工作站由智能手機連接直接控制,實驗數據可通過藍牙及時傳輸。迄今為止,絲網印刷技術對于SPE的制備已經成熟,因此SPE成本非常低。POCT檢測中靶標DNA的濃度選擇為10nM,以證明POCT微電化學工作站檢測SARS-COV-2變異株的可行性。如圖5所示,從SWV曲線得到的MB的氧化還原峰電流分別為933.05nA(不含靶標DNA)和280.11nA(含靶標DNA),ΔI%計算為69.97%,與從傳統電化學工作站獲得的相應ΔI%相比僅10%的差異。顯然,MoECS結合微型電化學平臺可用于POCT進行快速SARS-CoV-2 Delta變體的診斷,無需繁瑣的樣品處理。
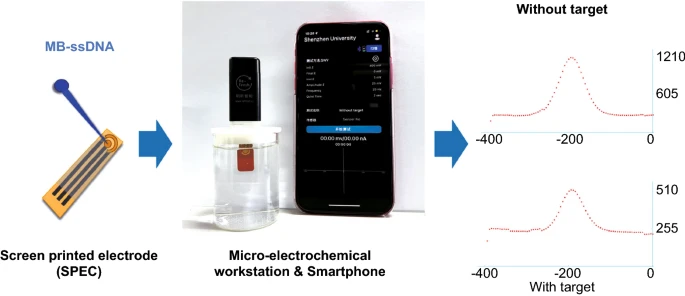
圖5 傳感器在POCT中用于SARS-CoV-2 Delta變異檢測的示意圖、初步分析照片和實驗結果。
論文鏈接: https://doi.org/10.1007/s40820-022-00888-4
審核編輯 :李倩
-
電化學
+關注
關注
1文章
325瀏覽量
20664 -
生物傳感器
+關注
關注
12文章
374瀏覽量
37425
原文標題:新型電化學生物傳感器,用于快速和超靈敏檢測新冠病毒德爾塔變異株
文章出處:【微信號:Micro-Fluidics,微信公眾號:微流控】歡迎添加關注!文章轉載請注明出處。
發布評論請先 登錄
相關推薦
安森美電化學傳感與無線傳輸解決方案助力遠程醫療
生物傳感器:科技前沿的生物監測利器
電化學氣體傳感器信號放大調試經驗
熱烈祝賀三郡科技電化學生物傳感電極芯片擴產能三億支
電化學測試方法詳解
關于電化學儲能的BMS可行性方案
電化學生物傳感器在生物檢測領域的顯著優勢
便攜快速檢測的電化學生物傳感器:顛覆性變革生物檢測方式
一種基于熵驅動雙足DNA walker的微米電極電化學傳感器
用于原位監測汗液標志物的全打印、多模態可穿戴生物傳感器陣列




 基于CRISPR-Cas系統的新型電化學生物傳感器
基于CRISPR-Cas系統的新型電化學生物傳感器










評論