背景介紹
與液態電解質或聚合物電解質不同,聚電解質(polyelectrolytes)是一種大分子,其骨架上含有可電離基團。這些可電離基團通過離子溶劑化分解成帶電物質(可移動的Li+和固定的陰離子)。Li+離子配位并與離子溶劑化基團如環氧乙烷(EO)形成配合物。鋰氧(Li-O)鍵的斷裂和形成促進了離子在聚電解質中的傳輸。隨著Li+溶劑化的配體逐漸被取代,連續的鏈段重排使得鋰離子的遠程位移成為可能。通過與聚合物基體的共價鍵錨定陰離子,使Li+成為系統中唯一的電荷載體,顯著緩解了上述低遷移數問題和安全問題。由于聚合物鏈的高柔韌性和與傳統固體電解質界面(SEI)形成添加劑的相容性,聚電解質具有更好的界面穩定性、可加工性和電化學穩定性。然而,它們的主要缺點是離子解離不足和鏈段弛豫緩慢導致離子電導率低。
成果簡介
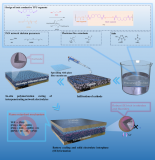
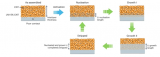
近日,加州大學歐文分校的忻獲麟團隊,利用無溶劑、紫外線誘導自由基聚合平臺,實現了由可電離單體、交聯劑和低聚聚乙烯氧化物增塑劑(PEG250)組成的前驅體溶液一鍋制得單離子(SIC)電解質(圖1a)。PEG250增塑劑的加入有效地促進了鏈段運動,玻璃化轉變溫度(Tg)從8.3℃顯著降低到-77.2℃。這種加速的鏈段弛豫降低了離子傳導的能壘和活化能,使得離子電導率在30℃時達到7.4×10-5S/cm,在60℃時達到1.9×10-4S/cm。此外,合成的SIC膜的遷移數為0.85,比具有相同聚合物化學性質但陰離子構型不同(圖1b,1c)的基準雙離子導體電解質(DIC,0.39)高出兩倍。SIC中高t+和均勻分布的陰離子使得臨界電流密度提高到2.4mA/cm2。相比之下,由于電極附近嚴重的濃度極化和鹽耗盡,基準DIC在0.8mA/cm2時經歷了軟短路。通過原位光學顯微鏡,可以觀察到SIC的高t+也促進了鍍Li0的光滑致密形貌的形成。低溫透射電子顯微鏡(Cryo-TEM)進一步揭示了Li0沉積的非枝狀納米形態,Li0球丘被致密的SEI層緊密保護。由于Li0的高t+和改進的形態穩定性,使用SIC的Li0||LiFePO4全電池在0.5C和室溫下表現出良好的4500次循環耐久性和70.5%的高容量保留率。
該成果以題目為“Anion-tetheredSingle Lithium-ion Conducting Polyelectrolytes through UV-inducedFree Radical Polymerization for Improved Morphological Stability ofLithium Metal Anodes”的文章發表在國際頂級期刊《AngewandteChemie》上。
01 圖文導讀
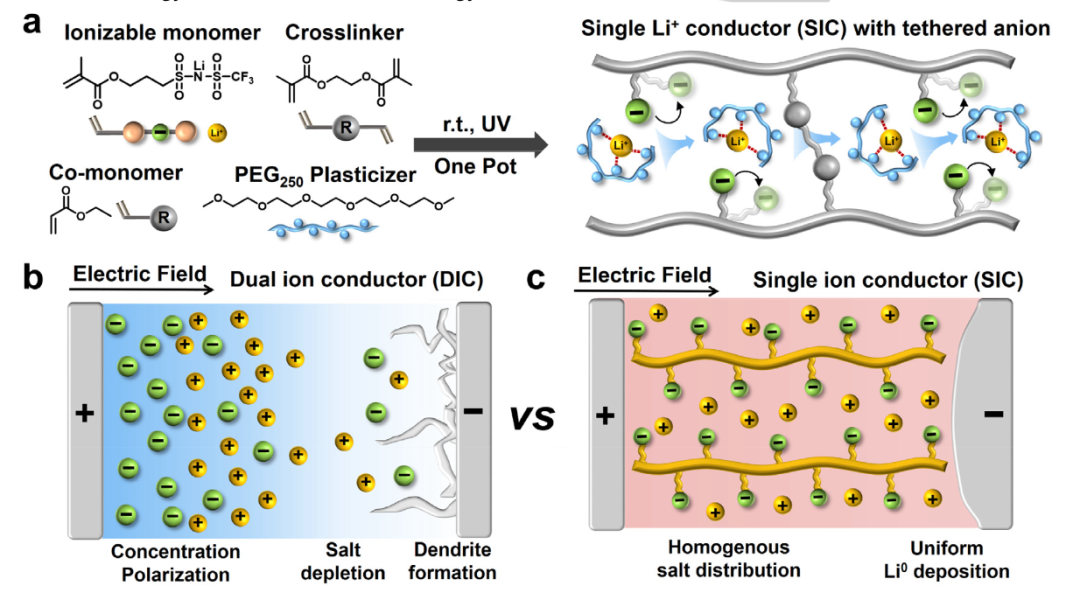
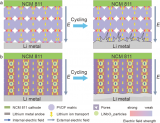
【圖1】設計概念。(a)紫外光聚合法合成單離子導體的示意圖。(b)常規DIC電解質由于濃差極化和鹽耗竭導致枝晶形成問題。(c)SIC電解質由于陰離子的均勻分布和高t+,提高了Li0負極的形態穩定性
SIC電解質的典型離子電導率比DIC低2-3個數量級,這主要是由于離子對的低解離和聚合物鏈段的緩慢弛豫。為了解決這一問題,引入無機或有機增塑劑能有效增強聚合物鏈的遷移率,促進離子傳導。PEG250是聚氧聚乙烯(PEO)的短鏈低聚物,對鋰鹽具有優異的溶劑化能力,其揮發性和可燃性更低。考慮到分子量與鏈段遷移率之間的關系,其中分子量降低導致鏈纏結減少和分子遷移率增加,較低分子量的PEG可以更有效地增強SIC主鏈的松弛并有助于提高電導率。為了在電導率和熱穩定性之間取得平衡,PEG的分子量選擇為250Da。
未塑化的SIC聚合物具有8.3℃的高玻璃化轉變溫度(Tg)。加入PEG250后,觀察到Tg顯著降低至-51.8oC(圖2a)。此外,將EO:Li摩爾比從5:1增加到21:1,使得Tg進一步降低到-77.2oC,表明聚合物的高遷移率可以降低離子傳導的能量壘。如圖2b所示,EO:Li比為20.9的SIC-3在30℃和60℃時的離子電導率分別為7.4×10-5S/cm和1.9×10-4S/cm。此外,離子電導率的溫度依賴性遵循Vogel-Fulcher-Tammann(VTF)方程而不是Arrhenius方程(圖2c),這表明聚合物鏈弛豫參與了離子傳導過程。隨著EO:Li比的增加,活化能從9.95降低到7.72kJ/mol(圖2d),這是由于鏈弛豫增強和Tg降低。因此,SIC-1的電導率從8.97×10-6S/cm增加到7.44×10-5S/cm。
為了研究陰離子構型對離子傳輸動力學的影響,采用相同的UV聚合方法合成了含有可移動Li+和可移動陰離子的DIC電解質。圖2a至2d顯示,DIC-1的Tg為-76.5oC,但在30oC時表現出更高的電導率2.35×10-4S/cm。VTF擬合分析進一步表明,活化能降低(7.30kJ/mol),指前因子A增加,這可能是由于缺乏外聚二離子基團導致鏈間相互作用減弱,離子對解離加快,從而提高了載流子的有效濃度。然而,盡管其電導率較高,但DIC-1的t+僅為0.39,這表明61%的電流由不參與氧化還原反應的陰離子攜帶(圖2e)。這與SIC-3形成鮮明對比,SIC-3的t+為0.85,這是由于陰離子在骨架上的共價束縛(圖2f)。SIC-3的高t+值表明可電離單體的高度聚合。總之,SIC-3選擇性傳輸氧化還原離子同時固定反陰離子的能力有望在改善Li0的電化學性能和調節沉積行為方面發揮關鍵作用。
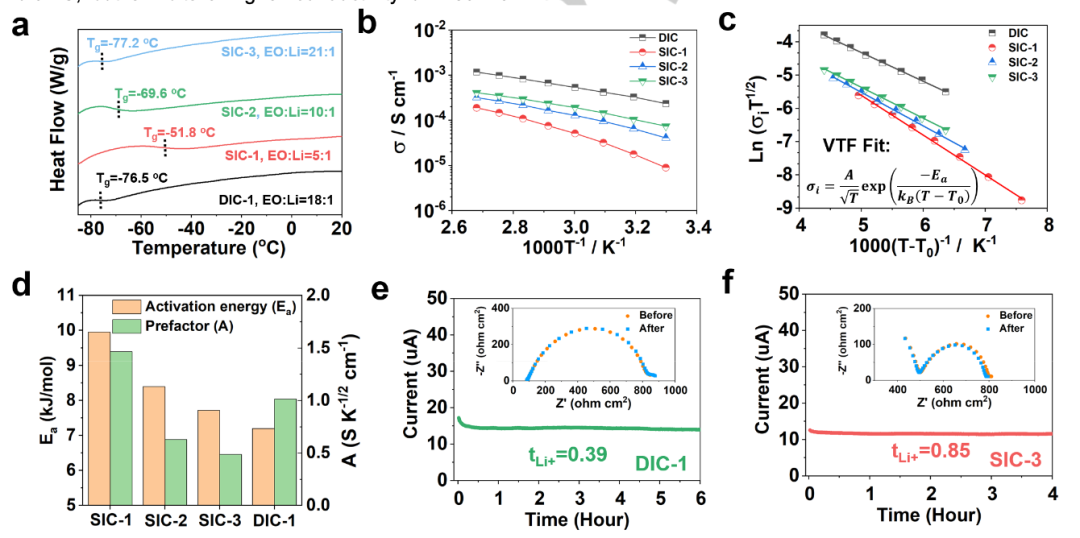
【圖2】SIC和DIC電解質離子輸運動力學。(a)不同EO:Li摩爾比下DIC和SIC電解質的玻璃化轉變溫度(Tg)。(b)在SS|電解質|SS的電池配置下,電化學阻抗譜(EIS)測試的離子電導率與溫度的關系,其中SS為不銹鋼阻斷電極。(c)研究離子通過SIC和DIC電解質傳導機理的VTF擬合結果。(d)VTF擬合得到的活化能Ea和指前因子A。(e-f)由Bruce和Vincent報道的靜電電位極化法測得的DIC-1電解質(e)和SIC-3電解質(f)的Li+轉移數(t+)
為了研究t+對電化學行為的影響,組裝了Li0||Li0對稱電池。隨后,在保持固定充電/放電時間為1小時的情況下,在電流密度從0.2mA/cm2逐漸增加到3mA/cm2的條件下循環電池,評估了SIC-3和DIC-1基電池的臨界電流密度(CCD)。SIC-3電解質顯示出2.4mA/cm2的高CCD(圖3a)。然而,盡管DIC-1電解質具有更高的導電性,但在0.8mA/cm2時導致電池失效(圖3b)。不同電流密度下的電壓-時間曲線如圖3c- 3e所示。對于DIC-1,在0.4mA/cm2充電時,電池電壓迅速從131mV上升到221mV。在更高的電流密度為0.8mA/cm2時,觀察到電池電壓呈指數增長,隨后出現電壓波動,表明電池內部存在微短路。當電池在極限電流密度以上運行時,通常會觀察到這種濃度極化引起的電池失效。當電流通過電解質時,陰離子在Li0剝離側附近積累,而在Li0電鍍側附近發生鹽耗盡。相比之下,具有共價束縛陰離子的SIC-3電解質在聚合物基體中均勻分布,最大限度地減少了陰離子的積累和鹽的消耗。
采用動態力學分析結果來研究電化學行為的偏差可以歸因于力學性能的差異。測量到的DIC-1和SIC-3的抗拉強度相似,分別為0.25MPa和0.26MPa(圖3f)。然而,與SIC-3相比,DIC-1具有更好的柔韌性,斷裂伸長率更高,達到1.5%。測定DIC-1和SIC-3的存儲模量分別為20MPa和60MPa,表明DIC-1比SIC-3具有更柔軟的性質(圖3g,3h)。總的來說,考慮到它們相同的交聯密度、Li+濃度和EO:Li比,DIC-1和SIC-3的力學性能是相似的。
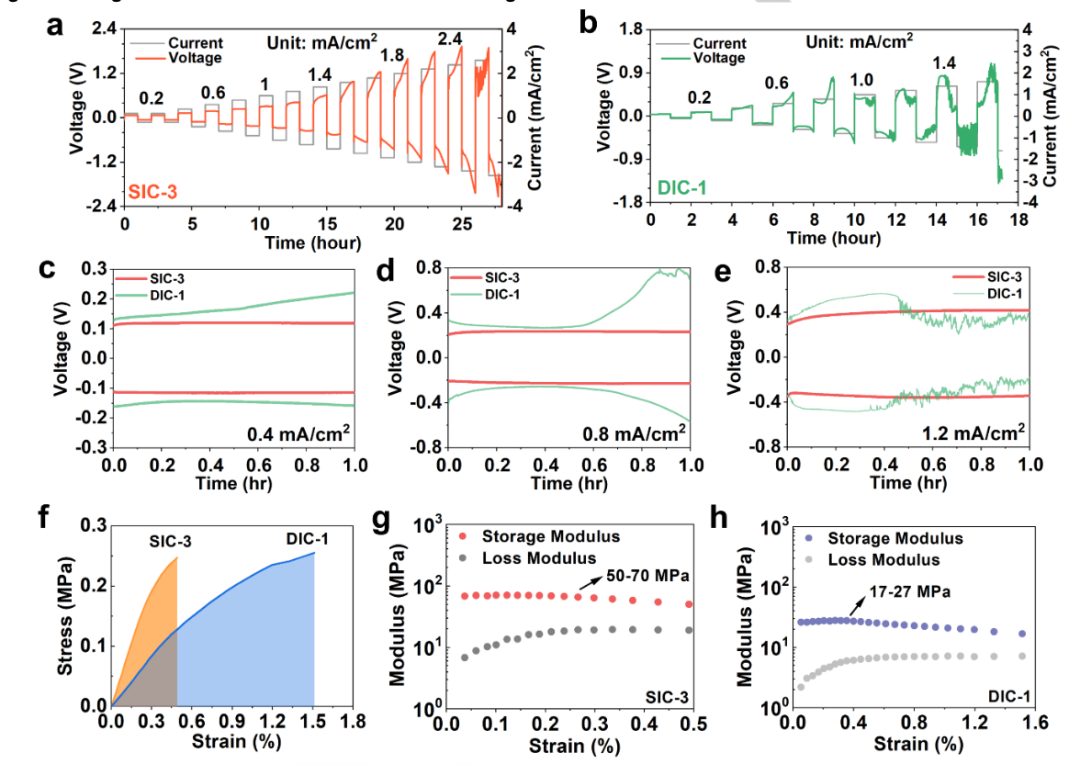
【圖3】臨界電流密度和機械性能。(a-b)SIC-3 (a)和DIC-1(b)電解質在50℃下測試的臨界電流密度,升壓電流密度為0.2-3mA/cm2,固定充放電時間為1小時。(c-e)不同電流密度下Li0|SIC-3|Li0和Li0|DIC-1|Li0電池在0.4mA/cm2(c)、0.8mA/cm2(d)和1.2mA/cm2(e)下的電壓-時間曲線。(f)動態力學分析測得的SIC-3和DIC-1電解質的抗拉強度和斷裂伸長率。(g-h)SIC-3和DIC-1的存儲模量和損耗模量
除了2.4mA/cm2的高臨界電流密度外,SIC-3電解質還可以穩定地鍍上Li0,高達3.6mAh/cm2的高面積容量(圖4a)。在0.2mA/cm2的恒流密度下充電18小時,Li0|SIC-3|Li0電池表現出穩定的過電位,由于SIC-3電解質的高t+,沒有觀察到明顯的濃度極化。與電壓-容量曲線一致,EIS曲線顯示體電阻或電荷轉移電阻沒有明顯變化(圖4b),表明沒有發生枝晶穿透或電極-電解質分層。另一方面,Li0|DIC-1|Li0電池在前3小時內出現了明顯的電壓升高,這可以歸因于陰離子遷移引起的濃度極化。此外,在4小時和0小時測量的EIS曲線保持不變(圖4c),排除了觀察到的電壓增加是由于電極-電解質分層或副反應引起的可能性。3小時后,電壓在15小時內從240mV降至100mV (3 mAh/cm2),EIS測量顯示電荷轉移電阻從900顯著降低到300ohm×cm2。這表明不均勻的枝狀Li0形態的發展,這可能導致電池內部的微短路。
為了驗證這一假設并揭示沉積Li0的宏觀形貌,原位組裝了光學電池。圖4d和4e顯示了0.2mA/cm2電鍍30小時前后的Li0電極的數字圖像。在DIC-1作用下,沉積的Li0呈現松散、不均勻、多孔的特征。相比之下,在SIC-3下鍍的Li0表現出致密非枝晶形態,具有閃亮的外觀,表明副反應最小。圖4f-4h進一步展示了掃描電鏡(SEM)圖像,顯示了Li0的微觀形貌。SIC-3實現了平坦、光滑、馬賽克狀的表面形態。這種形態可以減少孤立Li0的形成,并通過減少Li0與電解質之間的接觸面積來抑制副反應。相比之下,DIC生成的Li0沉積層顯示出細小的枝晶和松散堆積的顆粒,導致高度多孔且不均勻的形貌與原位光學電池表征一致(圖4h)。這種觀察到的Li0形態的差異進一步解釋了它們不同的電化學行為。DIC的低t+導致濃差極化和鹽耗盡,導致鋰枝晶的形成。
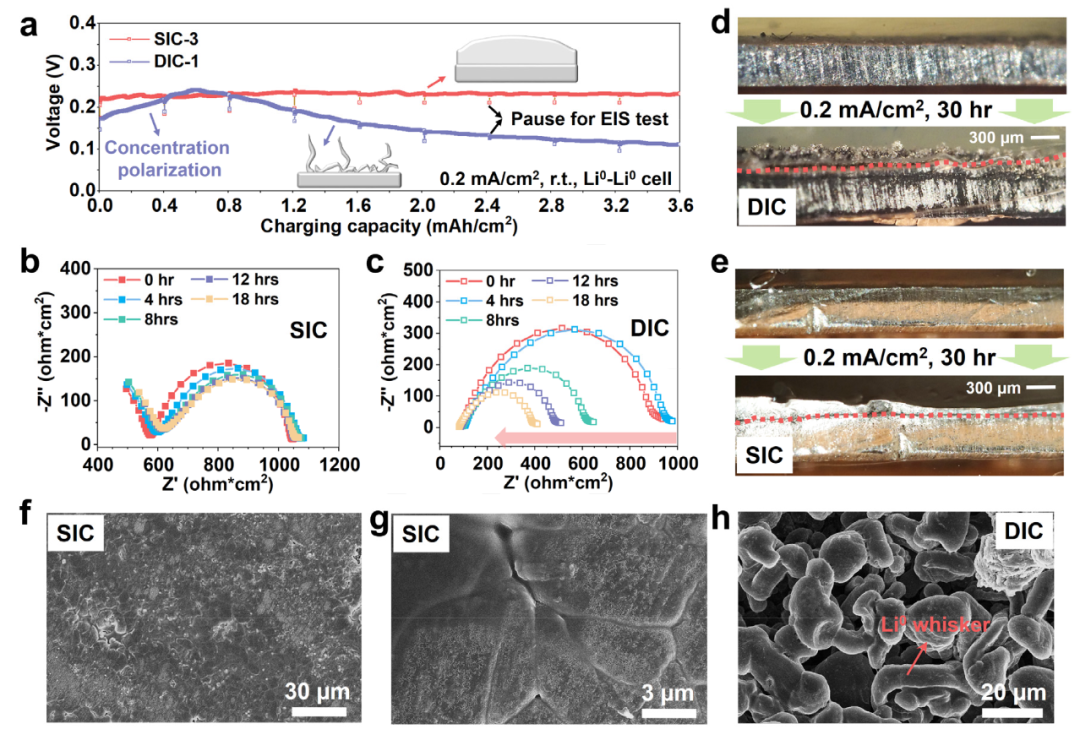
【圖4】Li0鍍層行為與形貌。(a)Li0|SIC-3|Li0和Li0|DIC-1|Li0對稱電池在0.2mA/cm2恒定電流密度下充電時的電壓容量分布圖。(b-c)Li0/SIC/Li0(b)和Li0|DIC|Li0電池(c)充電過程中EIS曲線的演變。(d-e)原位光學顯微鏡圖像顯示了在DIC-1(d)和SIC-3(e)電解質下鍍Li0的宏觀形貌。(f-h)SEM表征顯示了SIC-3(f,g)和DIC-1(h)電解質下鍍Li0的表面形貌
為了確認SIC-3電解質促進無枝晶鋰沉積的能力,采用多尺度低溫透射電子顯微鏡(Cryo-TEM)表征來研究沉積的鋰枝晶的形態和原子結構。如圖5a-5c所示,沉積的鋰的低溫透射電鏡圖像顯示出均勻堆積的球形鋰晶體,證實了不存在枝晶結構,并與非原位SEM結果一致(圖4f,4g)。圖5d為沉積鋰的代表性電子衍射圖(EDP),其中布拉格斑點對應于體心立方鋰金屬。鋰沉積物的原子分辨率低溫透射電鏡圖像(圖5e)和相應的快速傅里葉變換(FFT)(圖5f)表明,形成了由納米級結構域組成的SEI。低溫透射電鏡(Cryo-TEM)顯示,Li0沉積過程中枝晶結構的缺失和Li0沉積的均勻形貌為SIC電解質的電化學性能增強提供了進一步的支持。
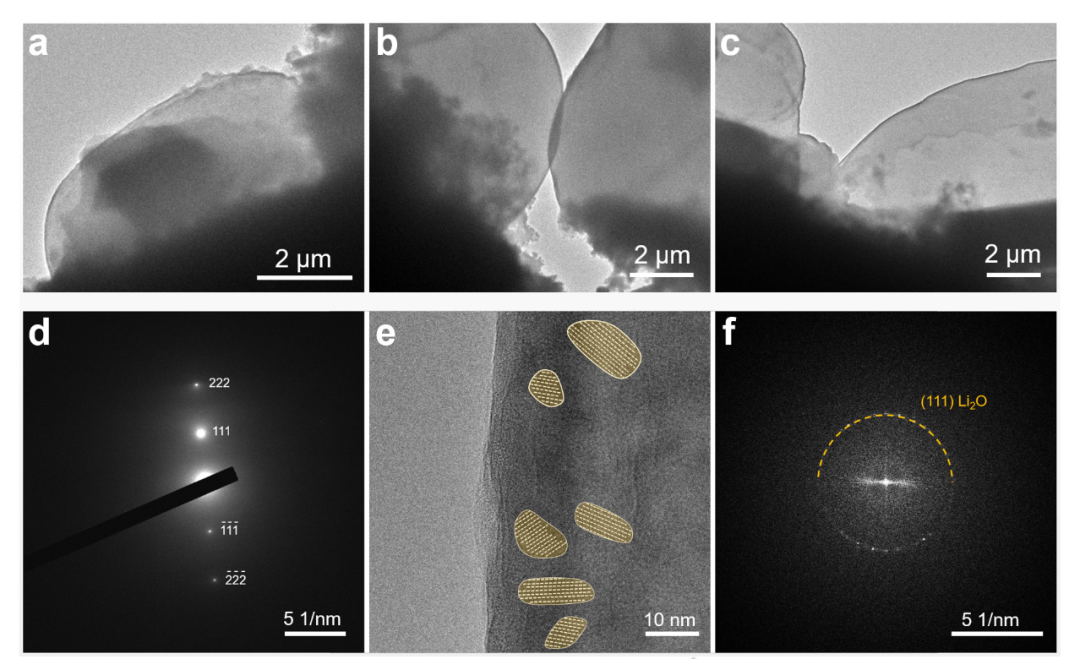
【圖5】Cryo-TEM表征。(a-c)具有代表性的低溫透射電子顯微鏡(Cryo-TEM)圖像顯示了具有SIC電解質的Li0沉積層的均勻球狀形貌。(d)沉積的Li0晶體的代表性電子衍射圖(EDP)。(e)具有代表性的原子分辨率低溫透射電鏡圖像,顯示了沉積的Li0的原子結構。(f)與(e)中原子分辨率低溫透射電鏡(Cryo-TEM)圖像對應的快速傅里葉變換(FFT)。識別出與(111)多晶Li2O晶體平面對應的衍射環
Li0|SIC-3|Li0電池的長期循環穩定性如圖6a所示。電池在0.2mA/cm2和0.2mAh/cm2下保持恒定過電位100mV,穩定工作1000小時。圖6b顯示了分別在2,500和1,000小時時提的電壓-時間曲線。低濃度過電位可歸因于SiC-3的高t+,使陰離子積累和鹽消耗量最小化。在循環過程中重疊的電壓-時間曲線表明電極和電解質之間沒有枝晶穿透或副反應的穩定界面。沒有觀察到電池電壓的波動或突然下降,表明在循環過程中沒有軟短路或硬短路。為了進一步證明電化學穩定性,在1mV/s的掃描速率下進行循環伏安法(CV)(圖6c)。在第一次掃描周期后,在電極上形成了固體電解質界面(SEI)層,在第2~ 4次掃描周期中,Li0鍍峰(還原)和Li0剝離峰(氧化)幾乎重合,證實了SIC-3與Li0之間的界面化學穩定。
在圖6d,6e中,以LiFePO4為正極組裝Li0負極全電池,其安全性高,成本低,穩定性好。在室溫和0.5C下,電池表現出良好的耐久性,循環次數超過4500次,容量保持率為70.5%。第1次、第1000次、第2000次、第3000次和第4000次的電池容量分別為135.5mAh/g、120.5mAh/g(89%)、115mAh/g(85%)、109mAh/g(81%)和102mAh/g(75%)。圖6d描繪了循環過程中的電壓-容量曲線,顯示了充電時3.53V和放電時3.34V的電壓平臺。經過12000小時的運行,過電位從195mV逐漸增加到401mV,這被認為是容量衰減的主要原因。值得注意的是,沒有觀察到微短路的跡象,證實了SIC電解質保持穩定界面化學和調節Li0沉積行為的能力。SIC-3電解質的良好耐久性可歸因于其足夠的Li+電導率(6.3×10-5S/cm)和適當的模量,在防止枝晶形成和避免電解質電極分層之間取得平衡。此外,由于高t+值、PEG250良好的Li0穩定性、無溶劑UV聚合合成以及FEC添加劑的SEI形成能力,使其具有穩定的界面化學性質,進一步提高了其整體耐久性。
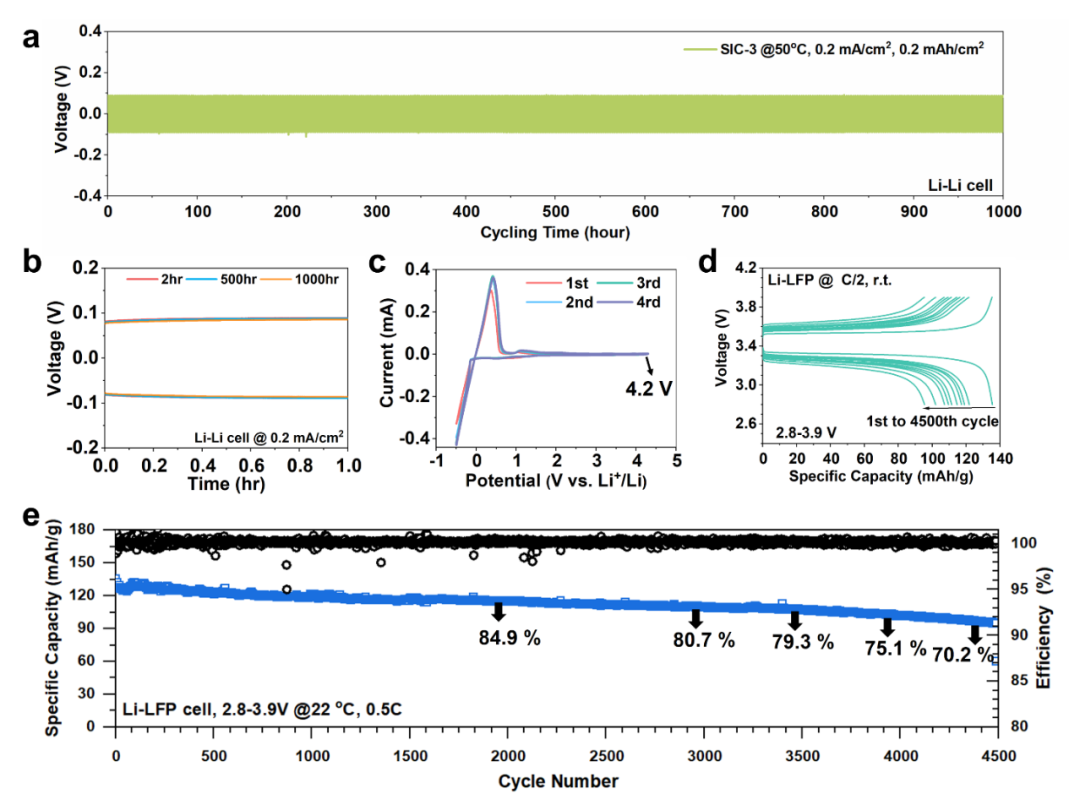
【圖6】鋰負極電池的實用性。(a)Li0|SIC-3|Li0電池在0.2mA/cm2、0.2mAh/cm2和50℃下的循環穩定性。(b)Li0|SIC|Li0電池工作2小時、500小時和1000小時時的電壓-時間曲線。(c)掃描速率為1mV/s時,Li0|SIC|SS配置下SIC-3電解質的CV曲線。(d)Li0|SIC|LiFePO4電池運行過程中,每500次循環所選電壓-容量曲線。(e)在室溫和C/2下測試的Li0|SIC|LiFePO4電池的長期循環性能。
總結與展望
在這項研究中,作者開發了一種具有高t+(0.85)的單離子化學。系統地研究了陰離子系縛對離子傳輸動力學、電化學性能和Li0沉積行為的影響。研究結果表明,離子通過SIC的傳導遵循VTF方程,聚合物鏈弛豫在決定電導率方面起著至關重要的作用。PEG250增塑劑的加入顯著增強了聚合物的鏈段運動(Tg為-77.2℃),降低了離子傳導的活化能(7.72kJ/mol),并實現了與DIC電解質相當的Li離子電導率(6.3vs 9.1×10-5S/cm)。由于沒有濃度極化和鹽耗盡,SIC電解質的臨界電流密度比DIC高3倍(2.4vs 0.8mA/cm2)。
此外,通過宏觀原位光學范圍、微觀尺度SEM和納米尺度冷凍透射電鏡表征,證實了SIC的高t+有利于致密、均勻和無枝晶的Li形貌。相比之下,在DIC下沉積的Li0表現出松散的多孔形態,帶有鋰枝晶,這可能導致電池短路。在Li0|Li0電池中,SIC電解液可以穩定循環1000小時,而濃度極化可以忽略不計,Li0|LiFePO4全電池在室溫下可以運行4500次。總的來說,本研究提供了形態學和電化學證據,支持單離子導電電解質的優勢,并強調在聚合物電解質或聚電解質的開發中需要同等重視t+和導電性。
審核編輯:劉清
-
CCD
+關注
關注
32文章
881瀏覽量
142294 -
電阻器
+關注
關注
21文章
3784瀏覽量
62150 -
電池電壓
+關注
關注
0文章
195瀏覽量
11701 -
電解質
+關注
關注
6文章
812瀏覽量
20068 -
電池充放電
+關注
關注
1文章
164瀏覽量
9047
原文標題:忻獲麟最新Angew:高鋰金屬負極形貌穩定性的聚電解質
文章出處:【微信號:清新電源,微信公眾號:清新電源】歡迎添加關注!文章轉載請注明出處。
發布評論請先 登錄
相關推薦
通過電荷分離型共價有機框架實現對鋰金屬電池固態電解質界面的精準調控




 高鋰金屬負極形貌穩定性的聚電解質
高鋰金屬負極形貌穩定性的聚電解質















評論