電解質工程是一種實現高性能鋰金屬電池的簡單而有效的策略,這是因為電解質溶液組分的溶劑化結構能夠起到調控電極/電解質界面的作用,對規整界面化學至關重要。
在這個工作中,我們首先發現了靜電相互作用對陰離子溶劑化結構的調控影響。陰離子和溶劑之間適度的靜電作用能夠促進了更多陰離子進入溶劑化鞘,從而在鋰金屬負極上形成穩定的固體電解質間相(SEI),同時兼具快速的Li?傳輸動力學效應。
高活性的鋰金屬負極和高電壓4.5 V的鈷酸鋰正極均在這種設計的電解質溶液表現出良好的兼容性。這項工作證明通過調節溶劑和陰離子的相互作用來優化溶劑化結構,可以實現高性能的鋰金屬電池。
?
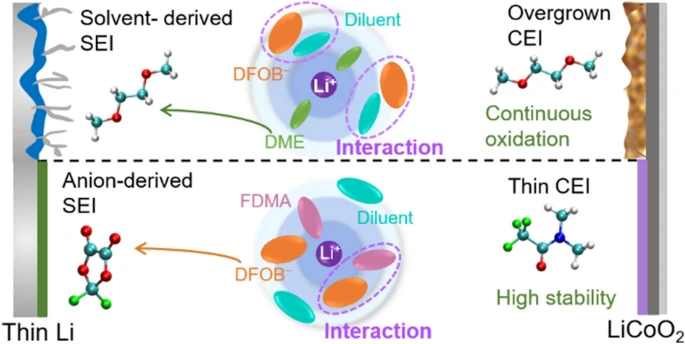
?
本文亮點
1. 首次提出電解質溶液中陰離子與溶劑分子之間的靜電作用,對調控溶劑化結構有著重要影響,這種作用區別于陰離子與稀釋劑分子之間的強相互作用。
2. 陰離子(DFOB?)和溶劑(FDMA)之間適度的靜電作用可以促進更多陰離子進入至溶劑化鞘(Anion-rich solvation),以誘導形成穩定的電解質-電極界面,同時兼具快速的Li?傳輸動力學效應。
3.電化學測試結果表明,在超過4.5 V的高電壓、15 μL的極低量電解質溶液和-20 ~ 60℃的寬溫度范圍等多種苛刻條件下,50 μm薄鋰與高負載LiCoO?組成的鋰金屬電池均具有出色的電化學性能。
內容簡介
眾所周知,在鋰金屬負極上形成穩定而均勻的固體電解質間相(SEI)可以解決鋰金屬電池(LMBs)的不可逆沉積和不可控的枝晶生長等問題,從而延長LMBs的壽命。然而SEI的結構和組成主要取決于電解質溶液中的Li?溶劑化結構,即Li?和溶劑分子或陰離子之間的微觀相互作用。清華大學深圳國際研究生院王賢樹博士和李寶華教授課題組,首次提出了陰離子和溶劑之間的靜電相互作用可以調控電解質溶液的溶劑化結構。他們設計了一種新型電解質溶液,即1 M二氟草酸硼酸鋰(LiDFOB)溶解在2,2,2-三氟-N, N-二甲基乙酰胺(FDMA)和1,1,2,3,3,3-六氟丙基-2,2,2-三氟乙基醚(HTE)的混合溶劑體系中。
根據分子動力學計算和表征測試的結果,發現DFOB?陰離子和FDMA溶劑之間適當強度的相互作用有利于構建富含陰離子的溶劑化結構。受益于這種獨特的溶劑化作用形成的高質量SEI,Li||Li對稱電池和Li||Cu電池都表現出高度可逆的鋰沉積/溶解行為,并且呈現出致密均勻的形貌學特征。此外,在高電壓、貧電解質和寬溫度范圍等工作條件下,由50微米鋰箔和高負載LiCoO?正極組成的LMBs表現出了優異的電化學性能。這項工作揭示了陰離子和溶劑之間相互作用調節電解質溶液溶劑化結構的基礎原理,為電解質設計工作提供了一個全新的視角。
圖文導讀
I 陰離子和溶劑之間的靜電效應
在這項工作中,含有1 M LiPF?-EC/EMC的商業電解質作為基礎電解液(Baseline),同時,在DME、FDMA、DME/HTE和FDMA/HTE中含有1M LiDFOB的電解質被分別表示為 "LiDFOB?DME"、"LiDFOB?FDMA"、"DDH"和"DFH"電解質。
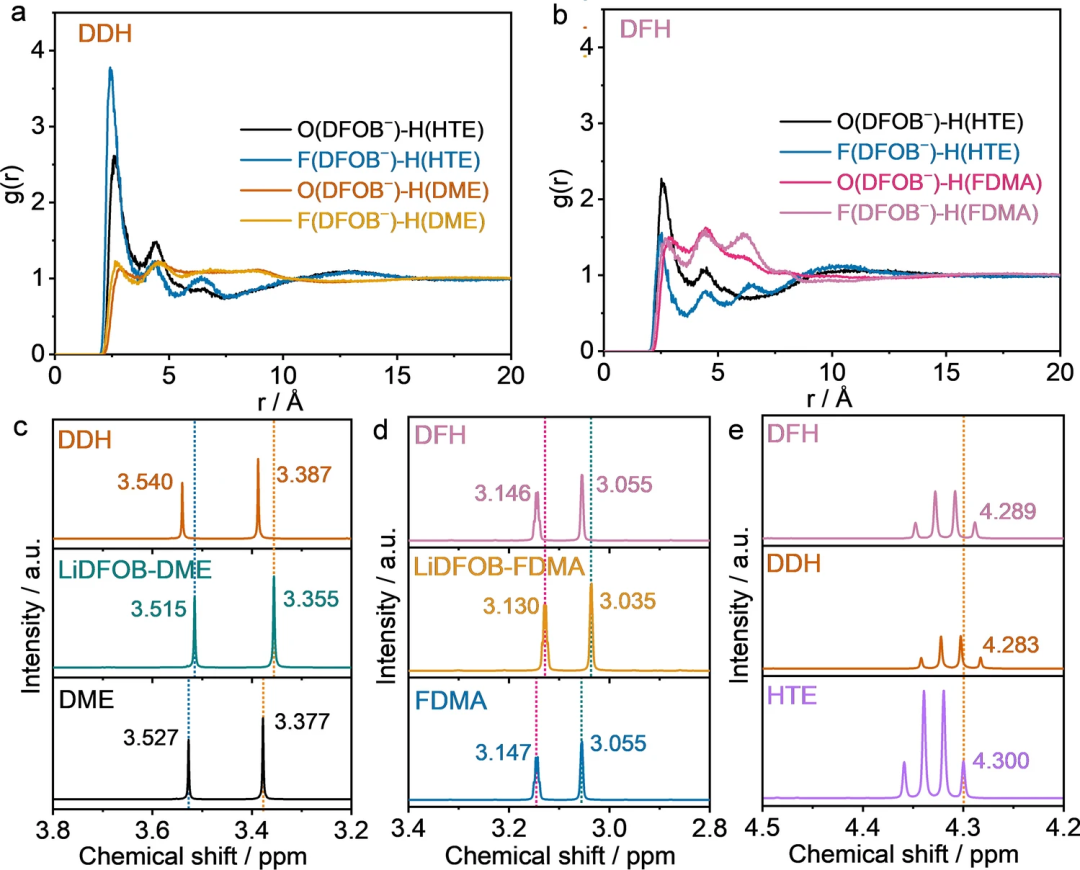
圖1. 陰離子和溶劑之間的靜電效應。(a, b) DDH和DFH電解質中陰離子和溶劑或稀釋劑分子之間的徑向分布函數;(c) 純DME溶劑、LiDFOB?DME和DDH電解質的1H NMR光譜;(d) 純FDMA溶劑、LiDFOB?FDMA和DFH電解液的1H NMR光譜;(e) 純HTE 溶劑、DDH和DFH電解液的1H NMR光譜。
首先,借助分子動力學(MD)模擬和核磁來研究電解質中陰離子和溶劑/稀釋劑分子之間的相互作用。在DDH電解質中,DFOB?陰離子和HHTE之間出現了強烈的靜電作用,而DFOB?陰離子和HDME之間的作用則相當弱(圖1a, b)。相比之下,DFH電解液中DFOB?陰離子和HHTE或HFDMA之間表現出強度相當的靜電作用。核磁結果也進一步驗證了在DDH電解質中,DFOB?陰離子容易與HHTE發生相互作用。而在DFH電解質中,陰離子對HFDMA和HHTE的相互作用幾乎是相等的(圖c-e)。
II 電解質的溶劑化結構的研究
一般來說,商業碳酸酯電解質的溶劑化結構主要由自由陰離子、溶劑分子和溶解的Li?陽離子組成。通過Li?徑向分布函數和拉曼光譜結果,可以看出,在DDH電解質中,內層Li?溶劑化鞘由大量的DME分子和少量的DFOB?陰離子主導,表現出典型的溶劑分離離子對(SSIP)主導的溶劑化結構(圖2a-c)。
而在DFH電解質中,溶劑化鞘由接觸離子對(CIP,一個DFOB?配位一個Li?)主導,并伴隨著一些聚集體(AGG,一個DFOB?配位兩個Li?或更多)。其中的HTE則與Li?無明顯配位,充當稀釋劑的角色。由此可知,在DDH電解質中,陰離子和HTE之間強烈的靜電作用使DFOB?陰離子只能停留在溶劑化鞘層外(圖2d)。而FDMA可以與陰離子作用,促使其接近內層,從而有助于形成一個富含陰離子的溶劑化結構(圖2e)。
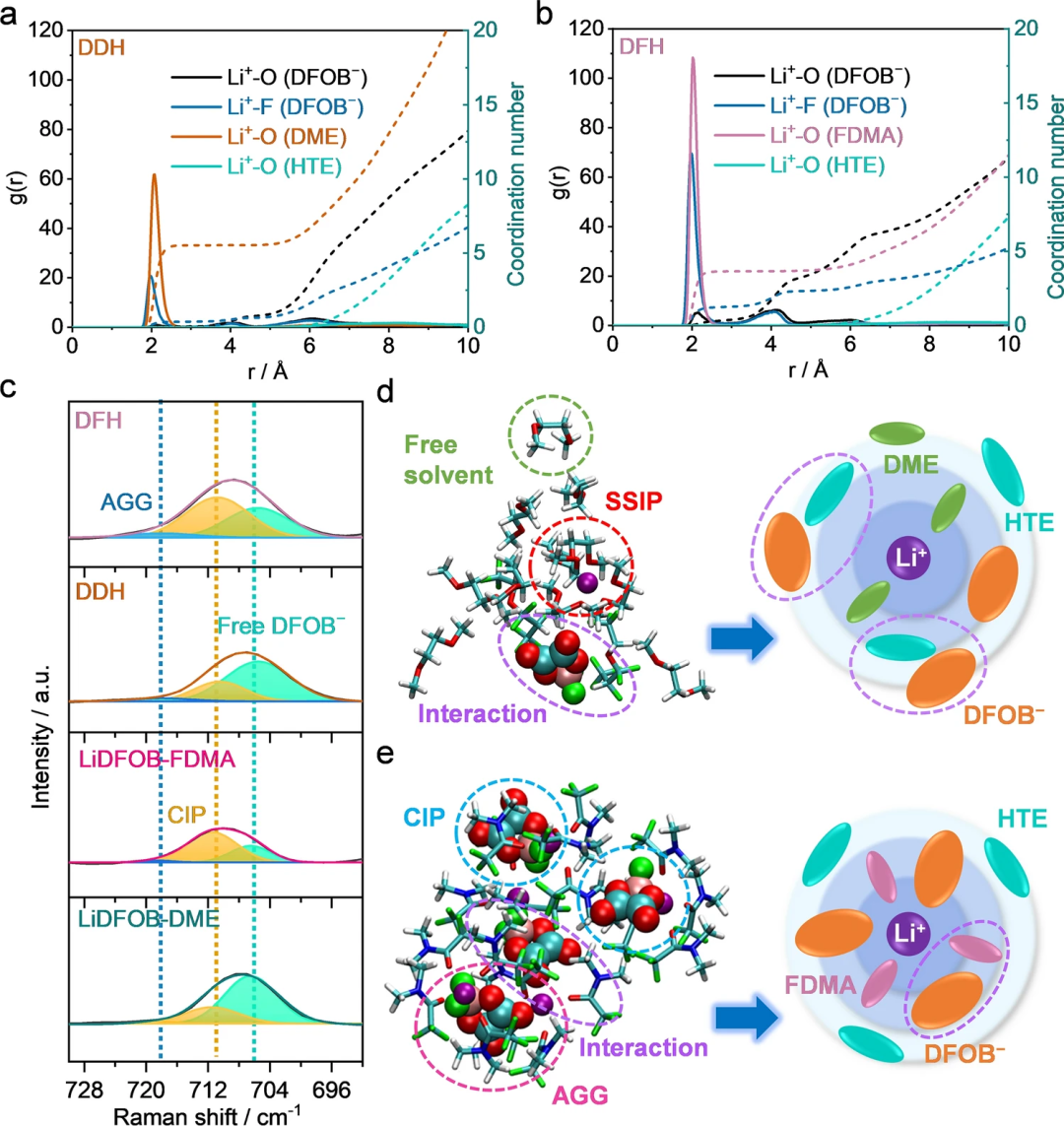
圖2. 電解質的配位溶劑化化學。(a, b) DDH和DFH電解質中的Li?徑向分布函數;(c) LiDFOB-DME、LiDFOB-FDMA、DDH和DFH電解質的拉曼光譜; (d, e) DDH和DFH電解質的Li?溶劑化結構以及對應的二維示意圖。
III 金屬鋰的形態和界面化學
在DFH電解質中,氟酰胺溶劑和Li?溶劑化鞘中的陰離子協同促進了溶劑化結構中Li?的快速解離,呈現出快速的動力學特征(圖3a)。DFH電解質與鋰負極表現出良好的相容性,實現鋰鋰對稱電池的750小時的長效循環,以及高達99.3 %的庫倫效率,且沉積形貌致密(圖3b-e)。
相比之下,商用電解液和DDH電解質僅能實現鋰鋰電池循環225小時和600小時,且庫倫效率均低于97%。這是由于富含DFOB?的Li?溶劑化結構有助于高機械強度和富含LiF組分的SEI層的形成(圖3f-i)。
?
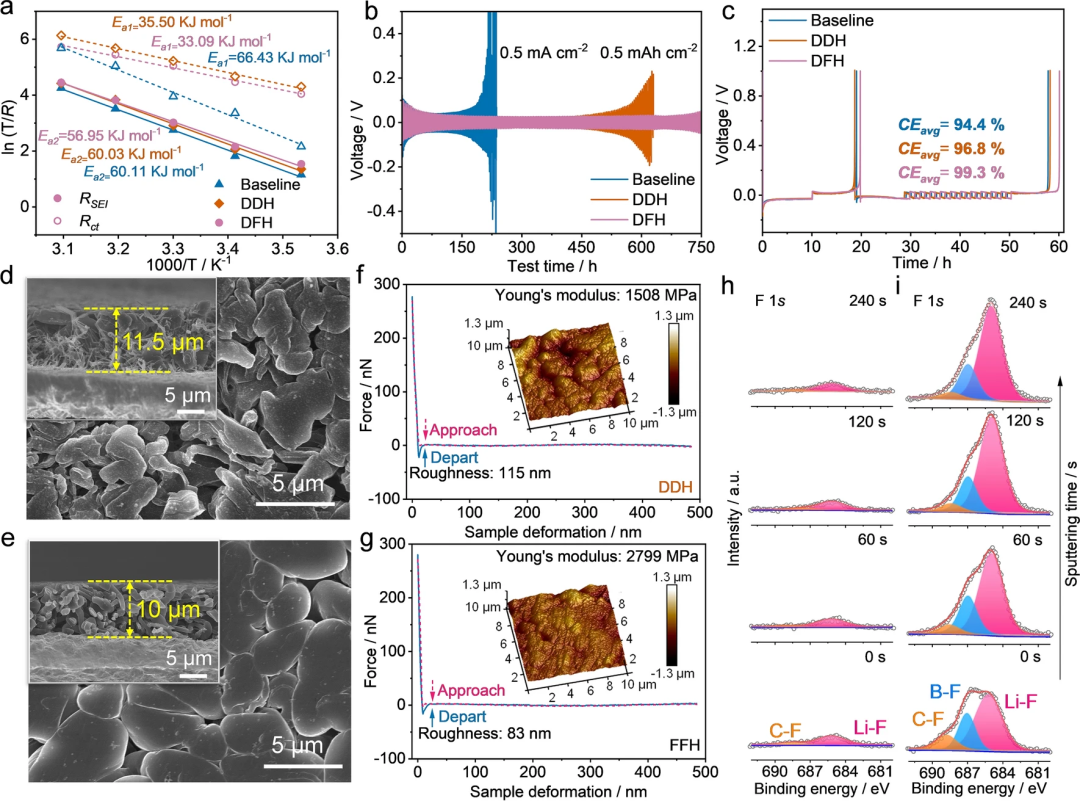
圖3. 鋰沉積/溶解行為和界面特征。(a) RSEI和Rct的活化能;(b) 不同電解質的Li||Li對稱電池在0.5 mA cm?2電流密度下循環的時間-電壓曲線;(c) 不同電解質的Li||Cu電池鋰沉積/溶解的CEavg測試;(d, e)使用DDH和DFH電解質,控制Li沉積于Cu箔的上的形貌學特征(FE-SEM圖像);(f, g) DDH和DDF電解質中鋰沉積的原子力顯微圖像,界面Young’s模量和粗糙度的對比;(h, i)使用DDH和DFH電解質的SEI層的F 1s深度剖析光譜。
IV 電化學性能評估 DFH電解液可實現Li||LiCoO?電池在0.3 C的倍率下穩定地循環達300次,容量保持率高達91%,且庫侖效率穩定在99.8 %(圖4a)。此外,充放電曲線表明在300個循環內使用DFH電解液的電池電壓下降和過電位均最小(圖4b),這與使用商用和DDH電解質中的過電位增長形成鮮明對比。
當電解液量從基本的60 μL減少到15 μL時,Li||LiCoO?電池在循環150次后仍然保持167.6 mAh g?1的容量(約初始容量的94%,圖4c)。同時,DFH電解質表現出優良的寬溫度性能,在60℃的高溫和-20℃的低溫下均表現出良好的循環性能(圖4d, e)。通過對比循環后電極表面可以證明,在DFH電解質中電極表面形成了更薄更均勻的CEI膜,抑制電解質的持續氧化分解,防止電極材料的結構破壞(圖4f-h)。
這項工作揭示了陰離子和溶劑之間的關系,以及其對溶劑化結構的影響,為LMBs電解質的設計開辟了新的方向。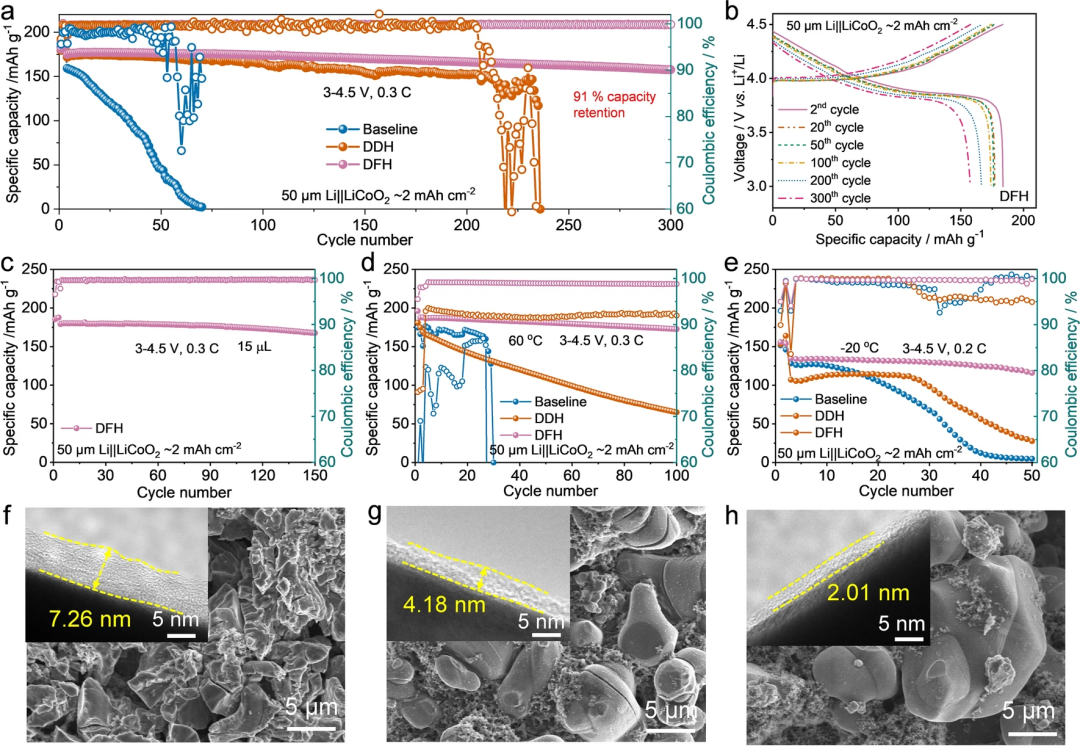
圖4. 鈷酸鋰全電池的循環性能
和循環后形貌。(a) 使用不同電解液的鈷酸鋰電池的長循環性能;(b) 使用DFH電解液的鈷酸鋰電池選擇性的充放電曲線;(c) 使用15 μL DFH電解液的鈷酸鋰電池的循環性能;(d, e) 使用不同電解液的鈷酸鋰電池在 60 ℃和 -20 ℃條件下的循環性能;(f-g) 鈷酸鋰正極在商用、DDH和DFH電解液中循環50次后的FE-SEM和TEM圖像。 ? ? ? ? ?
審核編輯:劉清
