研究背景
在金屬離子電池中,電解質(zhì)在運(yùn)輸金屬離子(如Li+)方面起著重要作用,但了解電解質(zhì)性能與行為之間的關(guān)系仍然具有挑戰(zhàn)性。近些年來(lái),通過(guò)改變?nèi)軇㈥庪x子、添加劑等的類(lèi)型和數(shù)量來(lái)改變金屬離子(M+)—溶劑、M+ —陰離子對(duì)和陰離子—溶劑之間的相互作用,從而調(diào)節(jié)電解質(zhì)的性能的研究受到了廣泛的關(guān)注。但是,溶劑-溶劑之間的相互作用卻很少被提及,因?yàn)檫@種相互作用被認(rèn)為是非常弱的,比M+—陰離子之間的離子-離子相互作用和M+—溶劑之間的離子-偶極子相互作用要弱1 - 2個(gè)數(shù)量級(jí)。但是,考慮到在商用電解質(zhì)(1 M)中,溶劑的摩爾數(shù)要比陽(yáng)離子和陰離子的摩爾數(shù)高10 ~ 12倍,因此,明確溶劑-溶劑之間的相互作用對(duì)電解質(zhì)性能的影響是很有必要的。
成果簡(jiǎn)介
近日,中國(guó)科學(xué)院長(zhǎng)春應(yīng)化所明軍教授通過(guò)核磁共振(NMR)等表征模擬發(fā)現(xiàn)電解質(zhì)中存在弱溶劑-溶劑相互作用且具有顯著的穩(wěn)定電解質(zhì)的功能。作者深入研究了碳酸乙烯脂(EC)溶劑在鋰離子電池電解液中的作用。發(fā)現(xiàn)EC溶劑可以通過(guò)弱的分子間相互作用穩(wěn)定線性碳酸鹽溶劑電解質(zhì),特別是碳酸二乙酯(DEC)電解質(zhì),增強(qiáng)Li+ (EC)x(DEC)y配合物軌道間的能量差,從而表現(xiàn)出較強(qiáng)的抗還原能力。該觀點(diǎn)在其他金屬離子電池(如Na+, K+)中得到了進(jìn)一步的驗(yàn)證,該發(fā)現(xiàn)對(duì)設(shè)計(jì)電解質(zhì)和深入理解電池性能具有重要意義。該工作以“Weak Solvent?Solvent Interaction Enables High Stability of Battery Electrolyte”為題發(fā)表在ACS energy letters上。
研究亮點(diǎn)
1、作者基于核磁等方法發(fā)現(xiàn)EC溶劑的引入可以與DEC溶劑形成弱的溶劑間相互作用以穩(wěn)定電解質(zhì)。
2、通過(guò)模擬計(jì)算認(rèn)為溶劑間的相互作用可以影響Li+ (EC)x(DEC)y配合物軌道之間的能量差(即ΔE = HOMO?LUMO),以提高電解質(zhì)的抗還原能力。
3、這種弱的溶劑間相互作用也存在于EMC基電解質(zhì)及K/Na離子電池的電解質(zhì)中,影響電解質(zhì)性能。
4、需要深入研究,進(jìn)一步量化溶劑-溶劑間的相互作用,以估計(jì)出通過(guò)相互作用強(qiáng)度穩(wěn)定電解質(zhì)的臨界值。
圖文導(dǎo)讀
由圖1b可知,當(dāng)加入EC至EC/DEC的摩爾比達(dá)到3/7時(shí),從透明溶液中可以判斷副反應(yīng)完全被抑制。在LiPF6存在的情況下,為了保證電解液的穩(wěn)定性,EC/DEC的摩爾比應(yīng)大于4/6,說(shuō)明LiPF6可以加速副反應(yīng)。該結(jié)果表明EC與DEC之間的弱溶劑-溶劑相互作用對(duì)鋰金屬的穩(wěn)定起決定性作用,而不是陰離子-溶劑相互作用。
在Li||Li對(duì)稱(chēng)電池和Li||Cu不對(duì)稱(chēng)電池中可以進(jìn)一步證明EC在DEC基電解質(zhì)中的必要性(圖1c,d)。我們發(fā)現(xiàn),當(dāng)電解液中EC/DEC的摩爾比小于4/6時(shí),電解液的不穩(wěn)定性在鋰沉積剝離過(guò)程中進(jìn)一步放大,可以觀察到較大的過(guò)電位以及電池快速失效(圖1c)。
相比之下,在EC/DEC的摩爾比達(dá)到4/6或更高時(shí)(圖1c),可獲得較低的極化(約22 mV)和超過(guò)250 h的循環(huán)壽命。Li / Cu不對(duì)稱(chēng)電池的初始庫(kù)侖效率也證實(shí)了上述結(jié)果(圖1d)。此外,Li||石墨半電池進(jìn)一步證明了EC在DEC基電解質(zhì)中的必要性,當(dāng)EC/DEC摩爾比增加到4/6或更高時(shí),與金屬鋰不相容的DEC電解質(zhì)會(huì)變得相容并表現(xiàn)出穩(wěn)定的循環(huán)壽命。這些結(jié)果表明,添加EC后,電解質(zhì)的穩(wěn)定性有很大提高。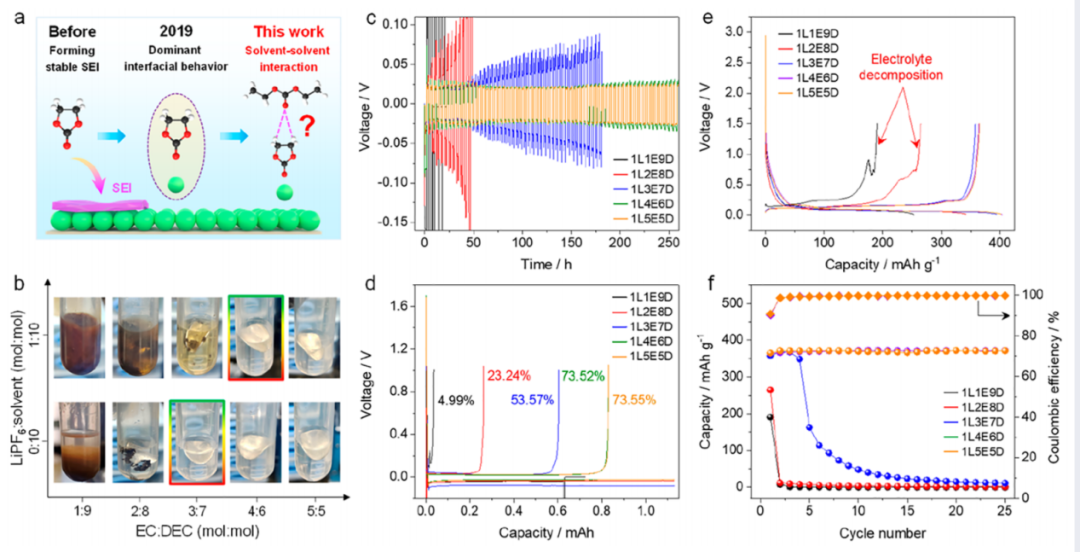
圖1. 不同溶劑-溶劑相互作用對(duì)電解質(zhì)穩(wěn)定性的影響:(a)對(duì)EC在電解質(zhì)中作用的認(rèn)識(shí)歷史;(b)金屬鋰在不同EC/DEC含量比例的電解液中的穩(wěn)定性比較;(c)在不同EC/DEC含量比例的電解液中的Li / Li電池的電壓/時(shí)間曲線, (d)Li/Cu半電池的相對(duì)的庫(kù)侖效率;(e)初始循環(huán)中的充放電曲線,(f)Li||石墨半電池的循環(huán)穩(wěn)定性。
在沒(méi)有LiPF6存在的情況下,我們發(fā)現(xiàn)添加EC溶劑時(shí),C=O上氧的化學(xué)位移向高場(chǎng)移動(dòng),而C?O?C上的氧峰沒(méi)有明顯的變化(圖2a)。這意味著EC和DEC溶劑可以通過(guò)富電子的O (δO?)和缺電子的H (δH+)進(jìn)行相互作用(圖2a所示),從而導(dǎo)致O上的電子云密度增加,表現(xiàn)出屏蔽效應(yīng)的增強(qiáng)。
當(dāng)EC和DEC溶劑混合時(shí),EC和DEC上H的化學(xué)位移在1H NMR譜上都向高場(chǎng)移動(dòng),這進(jìn)一步證明了EC和DEC之間存在δO?—δH+相互作用(圖3b)。C?O?C上可以忽略不計(jì)的氧的化學(xué)位移的變化表明這種溶劑-溶劑相互作用應(yīng)該是相對(duì)較弱的。
傅里葉變換紅外(FTIR)中,通過(guò)將EC/DEC的摩爾比從0/10增加到4/6,DEC分子的C=O峰的位置移向更低的波數(shù),此外,該峰的半峰寬也從26.8 拓展到31.7 cm-1。進(jìn)一步表明溶劑之間的弱相互作用(圖2c)。在LiPF6存在的情況下,EC /DEC的溶劑-溶劑相互作用更為明顯,因?yàn)樵贜MR譜中的C=O上的17O的峰位轉(zhuǎn)移到更高場(chǎng)(圖2d)。
這應(yīng)該歸因于電解質(zhì)中Li+-溶劑相互作用對(duì)溶劑-溶劑相互作用的誘導(dǎo)效應(yīng)。7 Li NMR譜中Li+化學(xué)位移的變化可以進(jìn)一步證明溶劑-溶劑相互作用的存在和影響,當(dāng)EC/DEC的摩爾比從1/9增加到4/6時(shí),7 Li化學(xué)位移向較低的場(chǎng)移動(dòng)(圖2e)。這一結(jié)果表明,Li+的屏蔽作用減弱了,它與溶劑分子的相互作用被減少。
此外,所有基于EC/DEC的電解質(zhì)的7Li化學(xué)位移均低于單一溶劑(即EC或DEC),充分說(shuō)明了溶劑-溶劑相互作用對(duì)Li+溶劑化過(guò)程的影響。在19F NMR譜中也可以觀察到同樣的趨勢(shì),其中所有基于EC/DEC的電解質(zhì)的19F的化學(xué)位移向低場(chǎng)強(qiáng)移動(dòng),并且比使用單一溶劑(即EC或DEC)的電解質(zhì)的19F的化學(xué)位移要低(圖2f)。
這說(shuō)明溶劑-溶劑相互作用減弱了Li+的屏蔽作用,提高Li+與PF6?之間的靜電相互作用,進(jìn)而增強(qiáng)了Li+對(duì)PF6?的去屏蔽作用。這種變化也證明了溶劑-溶劑相互作用的存在及對(duì)電解質(zhì)內(nèi)部結(jié)構(gòu)的影響。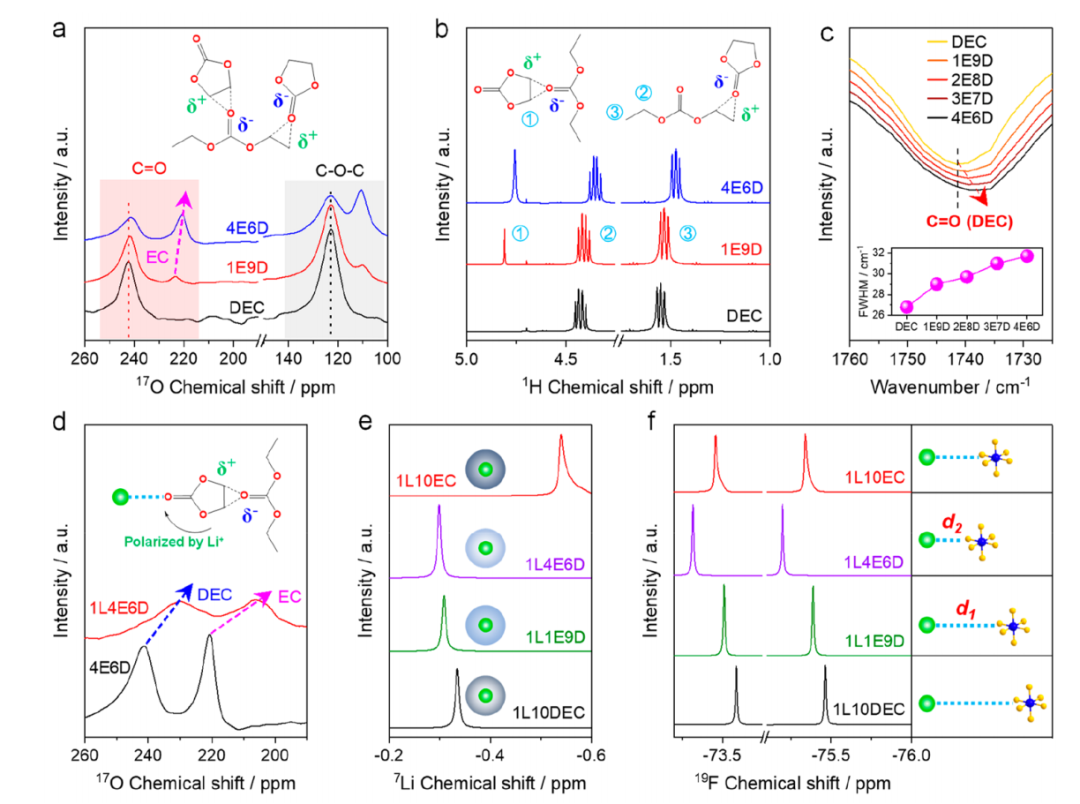
圖2. 弱溶劑-溶劑相互作用的光譜表征:(a) 17O核磁共振,(b) 1 H核磁共振,(c)含有不同量EC的EC/DEC混合溶劑的拉曼光譜;(d)加入LiPF6前后溶液的17O NMR譜;(e)含有不同量EC的EC/DEC基電解質(zhì)的7Li NMR和(f) 19F NMR譜。
在COSY 光譜中,發(fā)現(xiàn)EC?H與DEC?H之間的耦合概率隨著EC量的增加而增加,表現(xiàn)出更強(qiáng)的耦合信號(hào)(圖3a及b)。加入鋰鹽后,由于Li+對(duì)EC分子的極化作用,EC分子與DEC分子之間的弱溶劑-溶劑相互作用進(jìn)一步增強(qiáng)(圖3c),這大大增加了1 H?1 H耦合的強(qiáng)度,在COSY光譜中表現(xiàn)出額外增加的信號(hào)(圖3d及e)。
這一結(jié)果與7Li核磁共振譜相吻合。基于上述分析,電解質(zhì)的溶劑化結(jié)構(gòu)如圖3f及g所示。在1L1E9D電解質(zhì)(即LiPF6DEC = 19摩爾比)中,由于EC溶劑的不足,DEC溶劑仍然主導(dǎo)Li+溶劑化結(jié)構(gòu)的第一層,其中溶劑-溶劑相互作用也很弱。與之形成鮮明對(duì)比的是,在1L4E6D電解質(zhì)(即LiPF6DEC = 16摩爾比)中,EC足以占據(jù)Li+溶劑化結(jié)構(gòu)的第一層,其中EC—DEC的相互作用要比1L1E9D電解質(zhì)中的強(qiáng)得多。
因此,隨著EC— DEC溶劑間相互作用的增強(qiáng),Li+—溶劑相互作用被削弱,而Li+—PF6 -相互作用被增強(qiáng)。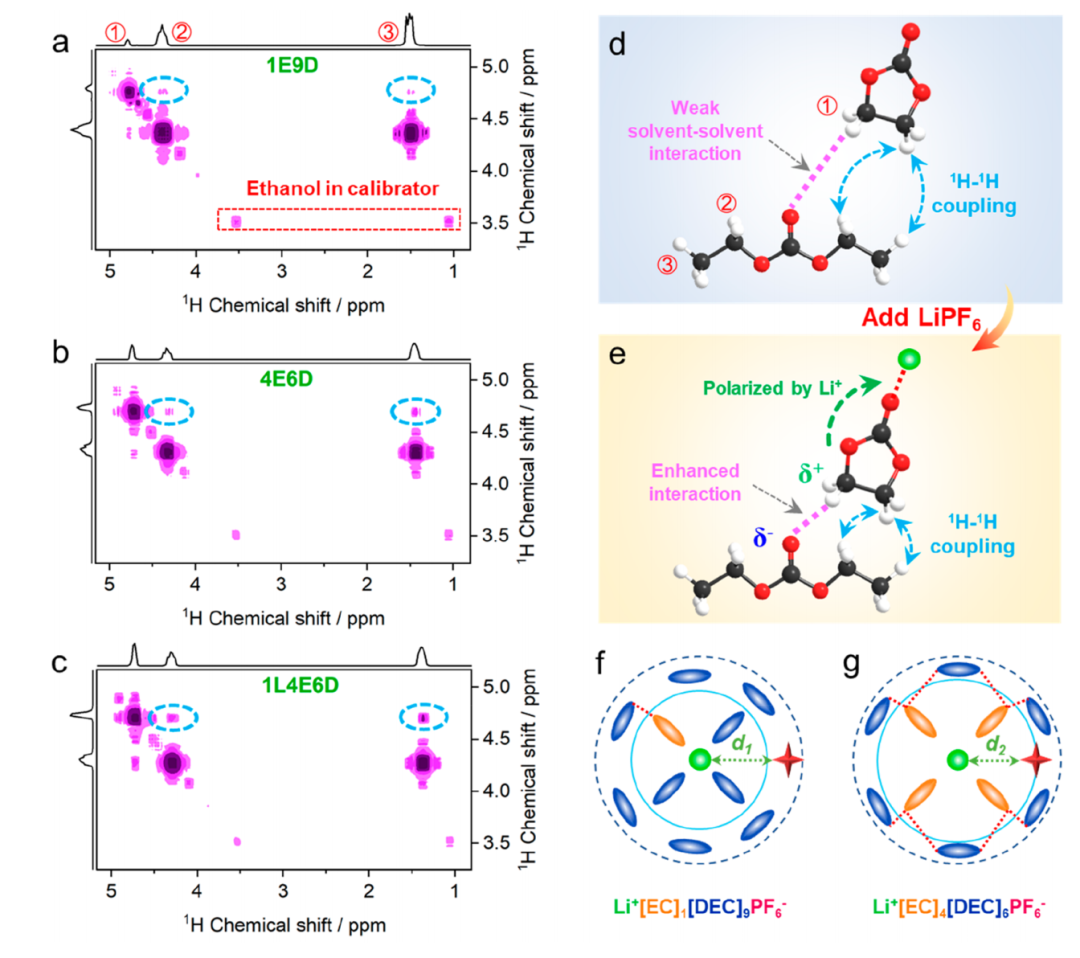
圖3弱溶劑-溶劑相互作用的二維1H—1H的COSY譜。(a) 1E9D, (b) 4E6D和(c) 1L4E6D電解質(zhì)溶液。(d, e)添加鋰鹽后耦合信號(hào)增強(qiáng)示意圖。(f) 1L1E9D和(g) 1L4E6D電解質(zhì)的溶劑化結(jié)構(gòu)示意圖。
模擬結(jié)果進(jìn)一步證明了在DEC基電解液中加入EC溶劑后,形成EC- DEC溶劑間相互作用的趨勢(shì)。首先,我們發(fā)現(xiàn)當(dāng)EC/DEC的摩爾比從0/ 10,1 /9增加到4/6時(shí),DEC出現(xiàn)在DEC周?chē)念l率變低(圖4a)。這意味著當(dāng)EC溶劑加入到DEC基電解質(zhì)中時(shí),EC分子可以取代DEC分子出現(xiàn)在DEC周?chē)纬蒃C—DEC相互作用。
此外,EC—EC、EC—DEC和DEC—DEC溶劑間相互作用的分子間作用力分別為?11.11、?8.90和?8.56 kcal mol?1(圖4b),數(shù)值非常接近,表明EC與DEC溶劑具有良好的混溶能力。這一結(jié)果進(jìn)一步證實(shí)了EC— DEC溶劑間相互作用的可能性。
此外,Li+ (EC)x(DEC)y配合物軌道之間的能量差(即ΔE = HOMO '?LUMO)被用來(lái)評(píng)估溶劑-溶劑相互作用的影響,其中最低的未占據(jù)分子軌道(LUMO)被用來(lái)表示Li+ (EC)x(DEC)y配合物的關(guān)鍵軌道,當(dāng)額外接收一個(gè)電子時(shí),相應(yīng)的軌道就變成了HOMO '(即Li0 (EC)x(DEC)y配合物)。Li+ (EC)x(DEC)y配合物(即x + y = 10)作為該模型的基本單位。軌道之間的能量差越大,電子轉(zhuǎn)移越困難,Li+ (EC)x(DEC)y配合物的穩(wěn)定性就越高。
當(dāng)EC/DEC的摩爾比從0/10,1/9增加到4/6時(shí),Li+ (EC)x(DEC)y的ΔE值從0.0636、0.0696增加到0.0767 Hartree (圖4c及d)。當(dāng)EC/ DEC的摩爾比增加到4/6或更高時(shí),電解質(zhì)就變得穩(wěn)定和或?qū)︿嚫嫒荨_@些結(jié)果表明,形成的EC—DEC的溶劑間相互作用對(duì)電解液的穩(wěn)定性有顯著影響。此外,作者在EMC溶劑及K/Na離子電池用電解質(zhì)中進(jìn)一步驗(yàn)證了這種溶劑-溶劑相互作用對(duì)電解質(zhì)穩(wěn)定性的影響。
作者認(rèn)為這些結(jié)果表明,在不同的電池體系中,當(dāng)溶劑的摩爾比和陽(yáng)離子的種類(lèi)(如Li+、Na+、K+等)發(fā)生變化時(shí),這種弱溶劑-溶劑相互作用也會(huì)發(fā)生變化。因此,需要深入該領(lǐng)域,進(jìn)一步量化溶劑-溶劑間的相互作用,以估計(jì)出通過(guò)相互作用強(qiáng)度穩(wěn)定電解質(zhì)的臨界值。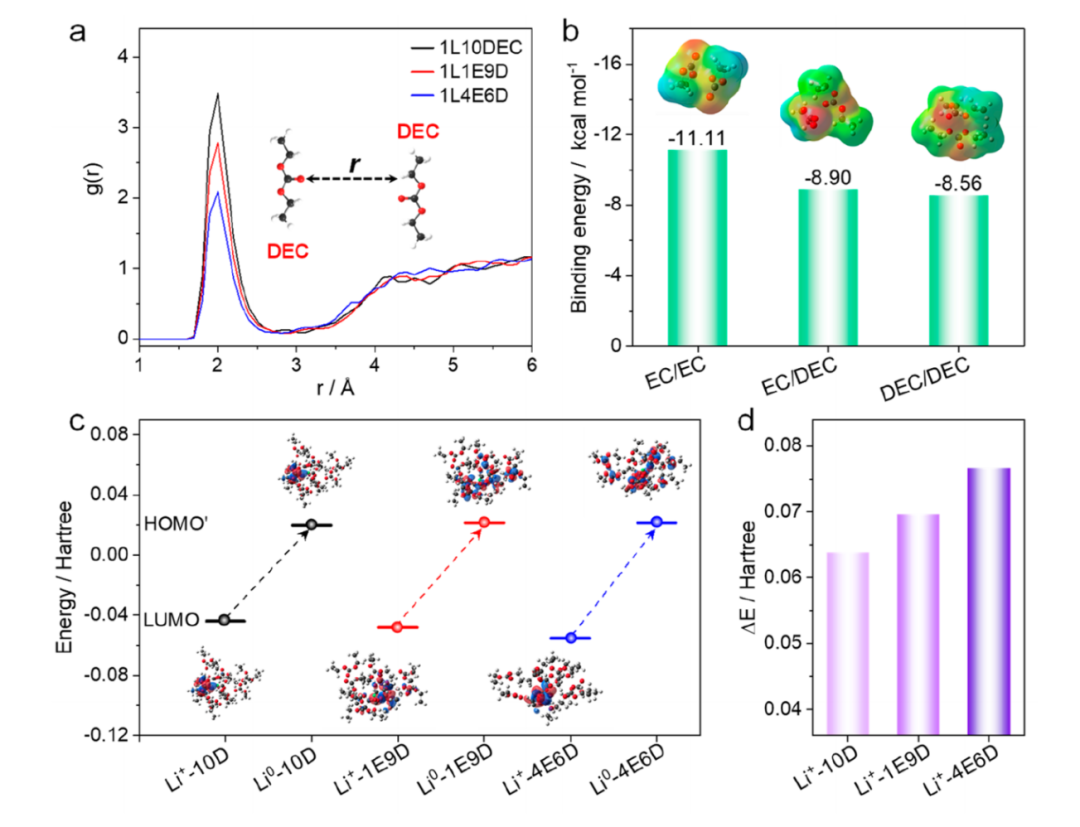
圖4。理論計(jì)算和模擬:(a)不同EC含量的EC/DEC基電解質(zhì)的徑向分布函數(shù)(RDF);(b) EC?EC、EC?DEC和DEC?DEC的結(jié)合能;(c)在(Li+)和(Li0)接受一個(gè)額外電子之前和之后的HOMO?LUMO示意圖以及(d)相應(yīng)的ΔE值。
總結(jié)與展望
以最常用的EC/ DEC基電解質(zhì)為例,EC-DMC的溶劑間相互作用不僅可以通過(guò)2D NMR檢測(cè)到,而且可以改變Li +(溶劑)x(溶劑)y和Li0(溶劑)x(溶劑)y軌道之間的能量差,從而影響電解質(zhì)的穩(wěn)定性。這一發(fā)現(xiàn)更新了對(duì)EC溶劑在電池電解質(zhì)中的作用的認(rèn)識(shí),不僅如此,這種溶劑-溶劑相互作用的效果也在其他類(lèi)型的電解質(zhì)和電池系統(tǒng)中得到了驗(yàn)證。這項(xiàng)工作揭示了弱溶劑-溶劑相互作用的重要性,這對(duì)未來(lái)在分子水平上設(shè)計(jì)高性能電解質(zhì)具有一定指導(dǎo)意義。
審核編輯:劉清
-
離子電池
+關(guān)注
關(guān)注
0文章
69瀏覽量
10334 -
充放電
+關(guān)注
關(guān)注
0文章
173瀏覽量
22022 -
emc
+關(guān)注
關(guān)注
170文章
4028瀏覽量
185117 -
電解質(zhì)
+關(guān)注
關(guān)注
6文章
821瀏覽量
20445
原文標(biāo)題:中國(guó)科學(xué)院長(zhǎng)春應(yīng)化所明軍教授ACS energy letters:弱溶劑間相互作用提高電池電解質(zhì)穩(wěn)定性
文章出處:【微信號(hào):清新電源,微信公眾號(hào):清新電源】歡迎添加關(guān)注!文章轉(zhuǎn)載請(qǐng)注明出處。
發(fā)布評(píng)論請(qǐng)先 登錄
相關(guān)推薦
超聲波焊接有利于解決固態(tài)電池的枝晶問(wèn)題
研究論文::乙烯碳酸酯助力聚合物電解質(zhì)升級(jí),提升高電壓鋰金屬電池性能

斯坦福大學(xué)鮑哲南/崔屹PNAS:高性能鋰金屬電池用單氟電解質(zhì)
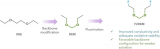
鉭電容對(duì)電路穩(wěn)定性的影響
陳軍院士團(tuán)隊(duì)最新Angew,聚合物電解質(zhì)新突破

Li3MX6全固態(tài)鋰離子電池固體電解質(zhì)材料
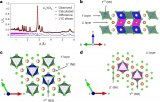
一種薄型層狀固態(tài)電解質(zhì)的設(shè)計(jì)策略
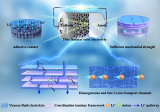
半互穿網(wǎng)絡(luò)電解質(zhì)用于高電壓鋰金屬電池
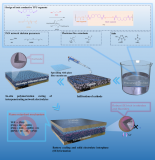
胡先羅教授在AEM發(fā)表研究:探索寬溫電解質(zhì)設(shè)計(jì)新路徑

固態(tài)電池中復(fù)合鋰陽(yáng)極上固體電解質(zhì)界面的調(diào)控

固態(tài)電池的安全性分析
無(wú)極電容器有電解質(zhì)嗎,無(wú)極電容器電解質(zhì)怎么測(cè)
提高電器應(yīng)用的TLC59283控制環(huán)路穩(wěn)定性

鈮酸鋰調(diào)控固態(tài)電解質(zhì)電場(chǎng)結(jié)構(gòu)促進(jìn)鋰離子高效傳輸!
眾多企業(yè)發(fā)布固態(tài)電池的布局動(dòng)態(tài)


















評(píng)論