在生命科學、深度學習、冷凍電鏡、細胞治療、分子模擬、蛋白質組學、疾病建模、靶點識別、藥物設計、AlphaFold的飛速發展下,中國醫藥研發領域、小分子研究領域得到飛速發展,已經成為全球第二大市場。
醫藥研發現狀及未來發展趨勢
我國生物醫藥研發支出累計環比增長
隨著醫改的穩步推進,傳統的以銷售為導向的擴張模式難以為繼,國內藥企面臨創新轉型。從2016年到2020年,生物醫藥上市公司的研發投入將繼續擴大。2020年,我國生物醫藥上市公司研發支出達到115.34億元,同比增長37.10%。2021年上半年,我國生物醫藥上市公司研發支出已達69.78億元,預計全年研發支出將進一步增加。總體來看,研發投入力度的增加將在一定程度上幫助企業加快生物醫藥產品的研究成果轉化。
我國新藥申請上市情況樂觀,新產品研發活躍
從轉化結果來看,我國新藥上市情況樂觀。2017-2020年,國內新藥申請上市數量呈波動趨勢,2018年達到峰值45件。2019年,藥審中心受理國內一類創新藥上市申請25個(16個品種),2020年上市申請43個。
創新藥物是指由企業或研究機構原創,具有新的化學結構和新的治療用途,并擁有自主知識產權專利的藥物。對特定疾病有顯著療效,提高治療率,延長患者生存期。在活動方面,國內生物制藥公司在研發活動中活躍。由于2020年新冠肺炎疫情爆發,有三家制藥公司已在新冠肺炎研發投資疫苗和檢測試劑。此外,另有藥企以人用疫苗和免疫球蛋白為主要研究方向。
我國創新藥物研究發展能力較強,投入及產出需改善
盡管中國生物醫藥產業研發投資和成果轉化較好,但與發達國家相比,中國創新藥物研發在許多指標上仍有待提高。在研發投入能力和產出方面,中國與發達國家存在一定差距。即使與水平相當的印度相比,新藥研發投入也有一定差距。目前,我國政府越來越重視自主知識產權創新藥物的研發,并出臺了一系列激勵政策,取得了一定的成效。但是,為了不斷提高我國創新藥物的研發能力,我國政府應不斷調整和完善相關政策,為我國醫藥企業創新藥物研發創造良好的政策環境。
我國創新藥物研發趨勢
雖然中國創新藥物的研發水平與世界領先國家相比還有很大差距,但未來,鑒于中國醫藥外包行業在世界上的領先地位和巨大的市場,中國有實力成為全球藥物創新中心,并且隨著新冠肺炎疫苗在國際上的日益普及,國家規劃對生物醫藥的高度重視,中國生物醫藥行業藥物研發未來可期。
AI技術為藥物研發帶來的變革與突破
在海量的知識點中,如何全面地尋找和評價決定性的關系和鏈接,如何建立相互作用,或者是推測關鍵待發現的知識點?從這個角度來看,人為學習的效率顯然是很低的。而AI從底層上來講,如果人工智能做到整個知識圖譜邏輯性的建立,AI去搜尋答案肯定比人為要強很多,并且AI具有搜尋地更全面更深入的優點。
藥物開發的各階段中,前期的基于疾病機理的靶點發現、生物標志物的發現、后期的臨床試驗設計、療效預測,目前都還基本處于數據收集分析,或者說大數據的時代。
由于缺乏足夠的經過驗證的結果,以及前期相對應的關聯數據,所以深度學習在缺乏足夠的數據和前期的成功的經過驗證的邏輯關系等限制條件下,還需要更多試驗數據和人本身認知的進步才有機會逐漸成熟。
但AI在某些臨床實踐中,諸如病理分析判斷等環節上應用的比較成功,也是因為積累了足夠多的數據和病理醫生的實踐經驗。但是從藥物開發的臨床設計和試驗數據收集環節來看,AI還沒到那個真正能突破的階段。相信未來隨著更多的臨床數據、大數據共享的普及,AI算法能夠脫穎而出。
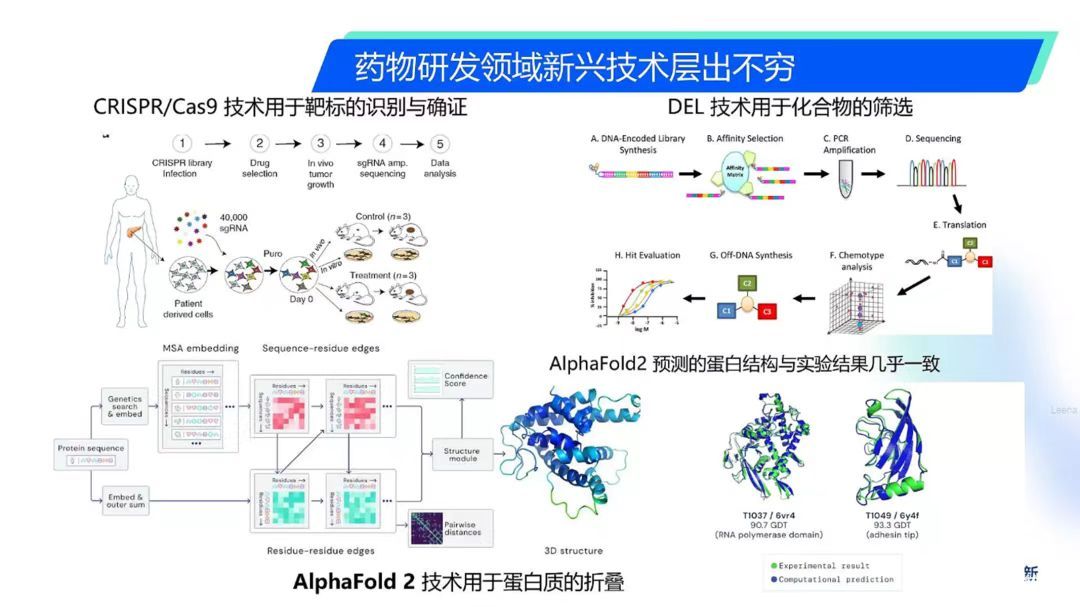
就目前來看,人工智能在藥物設計上,尤其是小分子,甚至大分子藥物設計上存在機遇。當然在蛋白藥物開發也存在一定的機遇,比如前一段時間AlphaFold出來之后,為蛋白序列、結構、蛋白質間的相互作用的研究提供了海量數據,隨著相關內在邏輯的理解逐漸深入,為AI驅動的深度學習提供了機會,將有可能真正實現突破。
在醫藥領域里,AI遇到的瓶頸
一、認知的局限和數據的質量
突破認知局限是更有挑戰的,高質量的數據可以通過聚焦的投入去生成。
二、人們對AI應用的理解
人需要理解規則,輸入輸出端一定的內在邏輯聯系,才能創造出好的AI應用。就像下棋,要打很多經典的棋譜才能做出AlphaGo。
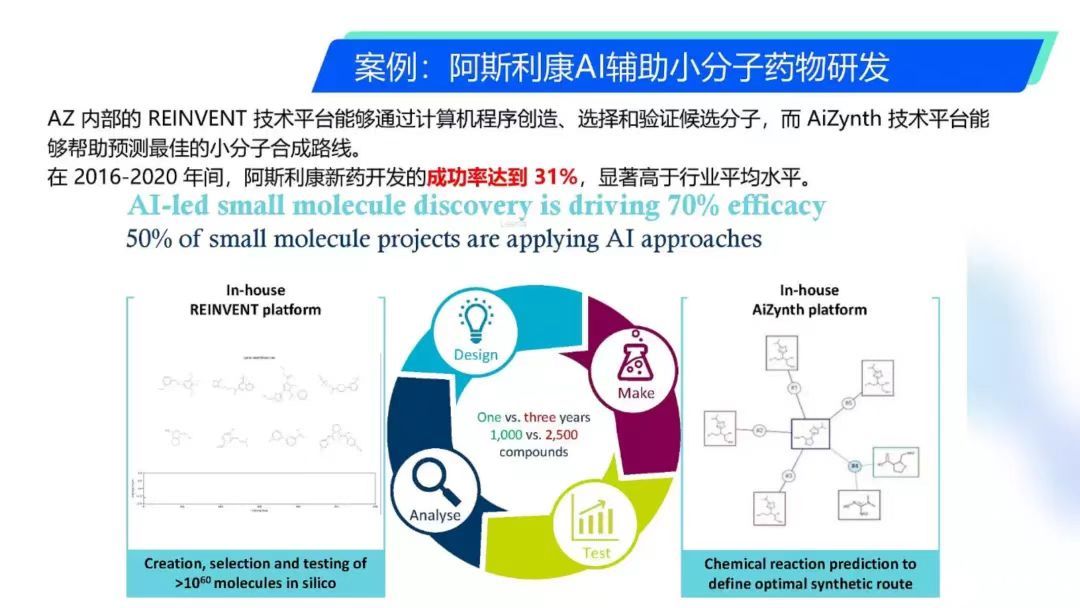
目前醫療領域前期的開發和后期的臨床數據解讀,都還不完善。但是在小分子和大分子結構及性質的數據上已經有了一定的積累,對分子序列,結構與一些分子特征,比如:親和力,成藥性等之間相互如何關聯的,AI對此如果有一定的認識將大有可為。
三、算法算力存在偏差
大公司很難釋放臨床數據,AI只是用現有的數據進行測算,這時數據大小和量會有限制。
四、數據樣本少
做臨床沒有太多的數據,做臨床一期也就是60位病人,二期200位病人,數據是非常有限的。無法使用有限的數據得到正確答案,這也是AI遇到的難題。
冷凍電鏡助力藥物研發
一直以來,科學家們都在探索基礎生命科學,探索細胞中的生命規律,為人類健康和其他學科提供參考。分子是生命中最小的單位,生命科學研究逐漸發展到微觀生物分子的結構和功能的研究階段,以逐步加深對生命過程的認知。充足的基礎研究不僅可以幫助我們深入了解生命過程,還有助于改善人類健康和生活質量。科學家可以通過生命科學研究幫助識別新藥靶點,并根據靶點進行藥物篩選,從而提高藥物研究的成功率、安全性和有效性。隨著生物制品,特別是抗體大分子的發展,冷凍電子顯微鏡越來越多地用于分析活性生物分子的結構。
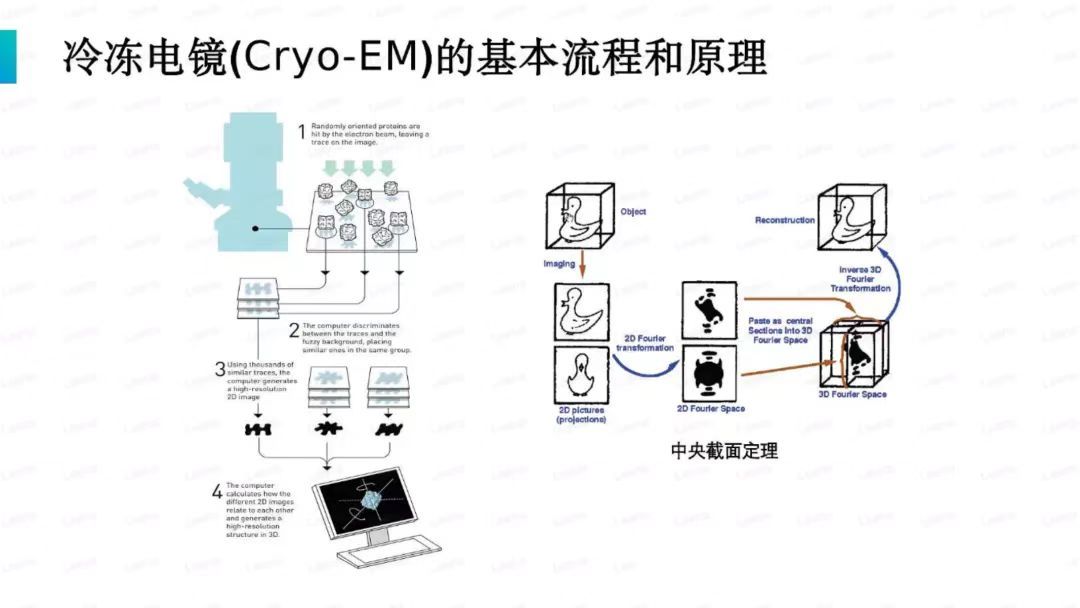
冷凍電子顯微鏡用于分析生物樣品的三維結構,包括單顆粒分析、微晶電子衍射和冷凍電子斷層掃描。冷凍電鏡單顆粒分析技術Cryo-EM SPA是一種以單個粒子形式分析生物分子組裝的新方法。通過快速冷凍負染電鏡獲得的適當濃度的生物分子樣品,生物大分子以近自然狀態存在于無定形冰中,然后對冷凍樣品進行篩選、數據采集和三維結構分析,獲得高分辨率的生物分子結構。其工作過程如圖。
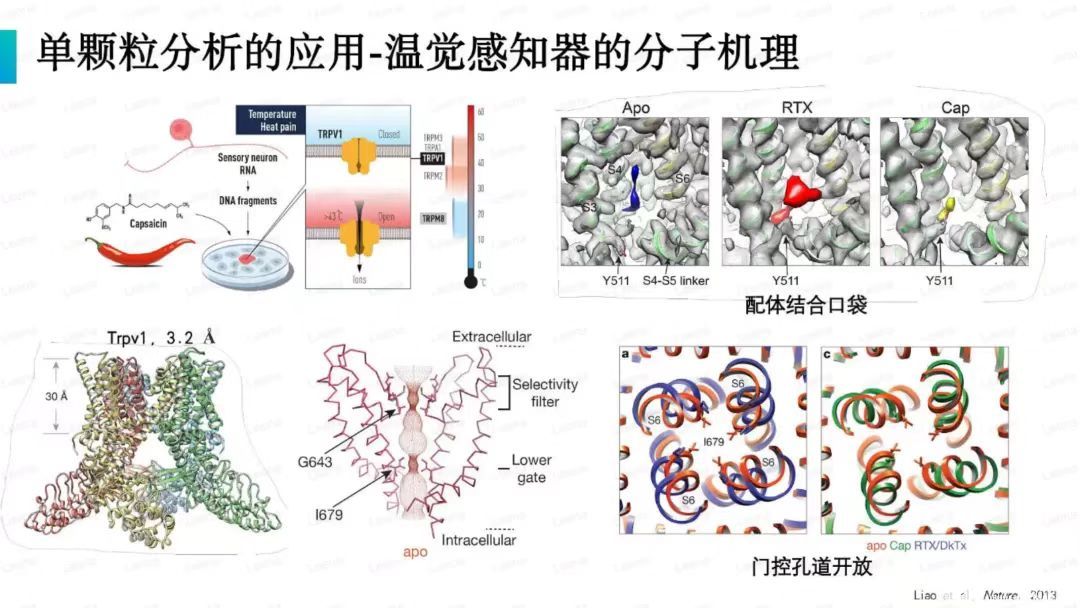
冷凍電鏡單粒子分析技術可以在分子水平進行細致的研究,分析基于結構的藥物研發的分子基礎,而冷凍電子斷層成像技術可以在亞細胞水平觀察原位細胞環境中靶分子的作用位點和作用機制,相信在不久的將來可以用于進一步確認基于結構的藥物研發的可靠性。電子衍射不僅可以分析小分子的微晶結構,還可以補充現有技術分析生物大分子及其化合物的微晶結構。
分子生物學興起后,靶向藥物發現逐漸成為主流的新藥研發模式。靶點-受體相互作用的靶和結合位點通常通過結構生物學方法獲得。以目標結構和結合位點為模型進行虛擬篩選,通過高通量方法獲得可能結合的潛在分子。此外,通過結構生物學方法直接分析目標潛在分子的高分辨率結構,并確認潛在分子。2014年,低溫電子顯微鏡的“分辨率革命”使其成為獲得3種以上結構的常規技術。高分辨率的結構可以清晰地描述靶分子和潛在分子之間相互作用的信息,包括結合表位、配體手性等。為潛在化合物的結構改造提供指導。
新的疾病或流行病爆發需要從頭進行藥物設計研究,而這些反應靈敏的藥物研發需要大量基礎研究的積累。冷凍電鏡技術不僅非常適合結構生物學的基礎研究,而且有助于加速結構藥物的研發。例如,在2020年新冠肺炎疫情期間,德克薩斯大學奧斯汀分校的Jason S. McLellan課題組和西湖大學的周強課題組先后分析了新型冠狀病毒跨膜刺突蛋白在膜融合前的細胞外結構域的三維結構和人類受體全長血管緊張素轉換酶2(ACE2)蛋白-新型冠狀病毒刺突蛋白復合物的近原子分辨率結構。不僅闡明了病毒感染人體的機制,而且促進了基于結構研究的合理疫苗設計和藥物研發,篩選出針對刺突蛋白的中和抗體候選物和重組疫苗候選物。
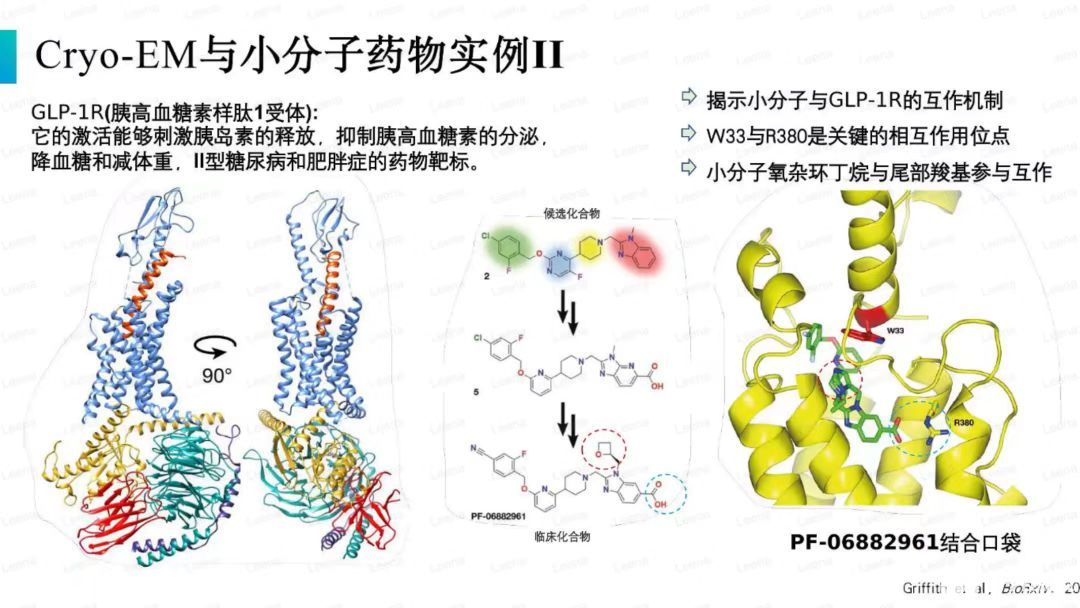
近年來,冷凍電鏡技術已被全世界公眾所熟知,并被越來越多的學術界和跨國制藥企業所采用。在藥物研發方面,許多跨國公司已經使用冷凍電子顯微鏡技術進行藥物研發。
雖然冷凍電鏡是一項前沿技術,但目前冷凍電鏡基于其結構研發的一些藥物已經進入臨床試驗階段。比如葛蘭素史克公司針對關鍵寄生蟲酶研發的新型黑熱病抑制劑,再生元制藥公司針對新冠肺炎研發的抗體“雞尾酒”,都已經進入臨床試驗階段。相信冷凍電鏡除了應用于基礎研究之外,還將越來越多地應用于藥物開發等其他研究領域,為人類健康做出貢獻。
冷凍電鏡未來的探索
冷凍電鏡技術在藥物研發過程中的應用實例進一步表明,該技術在藥物(生物制品)質量方面具有前瞻性意義。在回顧該技術應用的同時,我們也看到了冷凍電鏡在未來新藥研發中的發展方向。我們相信,冷凍電子顯微鏡將在基于結構的藥物設計、生物制劑的高級結構表征和冷鏈運輸過程中的質量控制中發揮越來越重要的作用。
藍海大腦助力藥物研發
案例概述
清華大學藥學院初始于2021年,藥物分子研發是一個非常復雜且非常耗時的過程,藥物分子篩選只是前期流程中的一個環節。如尋找跟蛋白病毒酶結合的小分子,由于存在不同種類或研究機構的配體(小分子)庫,配體(小分子)庫數量巨大,每個配體庫的配體數量成千上萬(甚至更大),通過實驗方式測試驗證是不切實際的。通過計算機數值模擬進行篩選,對不同配體的結合效果進行打分,篩選出分數高且結合模式合理的一些配體作為候選藥物進行實驗驗證,能夠有效的加速藥物研發進程。
由于配體庫數量巨大,在有限時間內完成篩選,同樣挑戰巨大。例如,配體庫有10000個候選配體,每個配體平均處理時間為1.5小時,總共需要15000 個小時(625天)。因此,為在規定時間內算完,需要具備以下條件:
一、擁有強大算力的計算平臺;
二、大容量存儲,用于存放處理數據和計算結果;
此外,為了保證篩選計算能夠高效、順利完成,還需要計算服務,包括:
一、集群軟件運行環境,保證在多機環境軟件下運行,以及數據訪問;
二、能夠支持多任務在多機環境下并發處理的并行方案。
除計算平臺外,藥物篩選還需要高性能應用軟件。藥物篩選模擬計算包括Docking和分子動力學計算:其中Docking 耗時相對較小,常用于大量配體的初步篩選,主要軟件有dock6、Autodock Vina、Glide等。分子動力學模擬計算比較耗時,測試作用的時間變化,用于對Docking初選結果進一步分析,主要軟件有Gromacs,Namd,Amber等,使用GPU加速效果一般比較明顯。
方案與價值
藥物小分子研發需要強大算力的高性能集群,獲取這些計算資源和服務成為當下的重中之重。清華大學藥學院搭建了四臺A100液冷服務器、9臺CPU服務器、兩臺高通量液冷服務器,為高性能計算環境提供基礎的計算平臺。
使用DOCK6 處理配體(小分子)庫的對接案例時,在一個文件夾中,如mol2,存放大量的小分子文件,每個小分子處理流程是一樣的,均需要與相同的受體(如病毒蛋白酶)進行計算。這時需要在短時間內提供大量GPU和超算產品,以及全天候的技術支持。搭建開放共享平臺,使用高性能計算集群,用于藥物研發的分子對接、分子動力學模擬、深度學習模型訓練,把需要幾天的計算工作縮短到幾小時,速度提升8到20倍。同時為各研發老師創建不同的子賬戶,實現計算資源共享和數據共享。為高性能計算環境提供基礎的計算平臺,要實現高效的藥物篩選,還需要高通量任務解決方案。
總結
清華大學藥學院藥物研發需要強大算力的高性能計算集群,如藥物篩選需要進行大量小分子的Docking處理。藥學院老師可以利用藍海大腦高性能液冷服務器,快速構建高性能集群,獲取高性能的計算實例,滿足算力的需求。同時提供高通量任務處理的解決方案,使得藥物篩選在多計算節點、多核上并發處理,降低任務整體執行時間。
審核編輯:符乾江
-
人工智能
+關注
關注
1794文章
47642瀏覽量
239678 -
生命科學
+關注
關注
0文章
24瀏覽量
12379
發布評論請先 登錄
相關推薦
借助NVIDIA AI Foundry平臺推動醫療健康與生命科學行業發展
NVIDIA攜手多家機構推動醫療健康產業變革
tga熱重分析儀在醫藥領域的應用

施耐德電氣助力生命科學與電子行業的可持續發展
施耐德電氣助力生命科學行業高質量發展
AI for Science:人工智能驅動科學創新》第4章-AI與生命科學讀后感
名單公布!【書籍評測活動NO.44】AI for Science:人工智能驅動科學創新
激光引擎改善生命科學應用
NVIDIA AI微服務現已與AWS集成,加速藥物研發和數字醫療
合肥高新區與雪湖科技簽署生命科學超算總部項目,聚焦生物科技和新材料領域
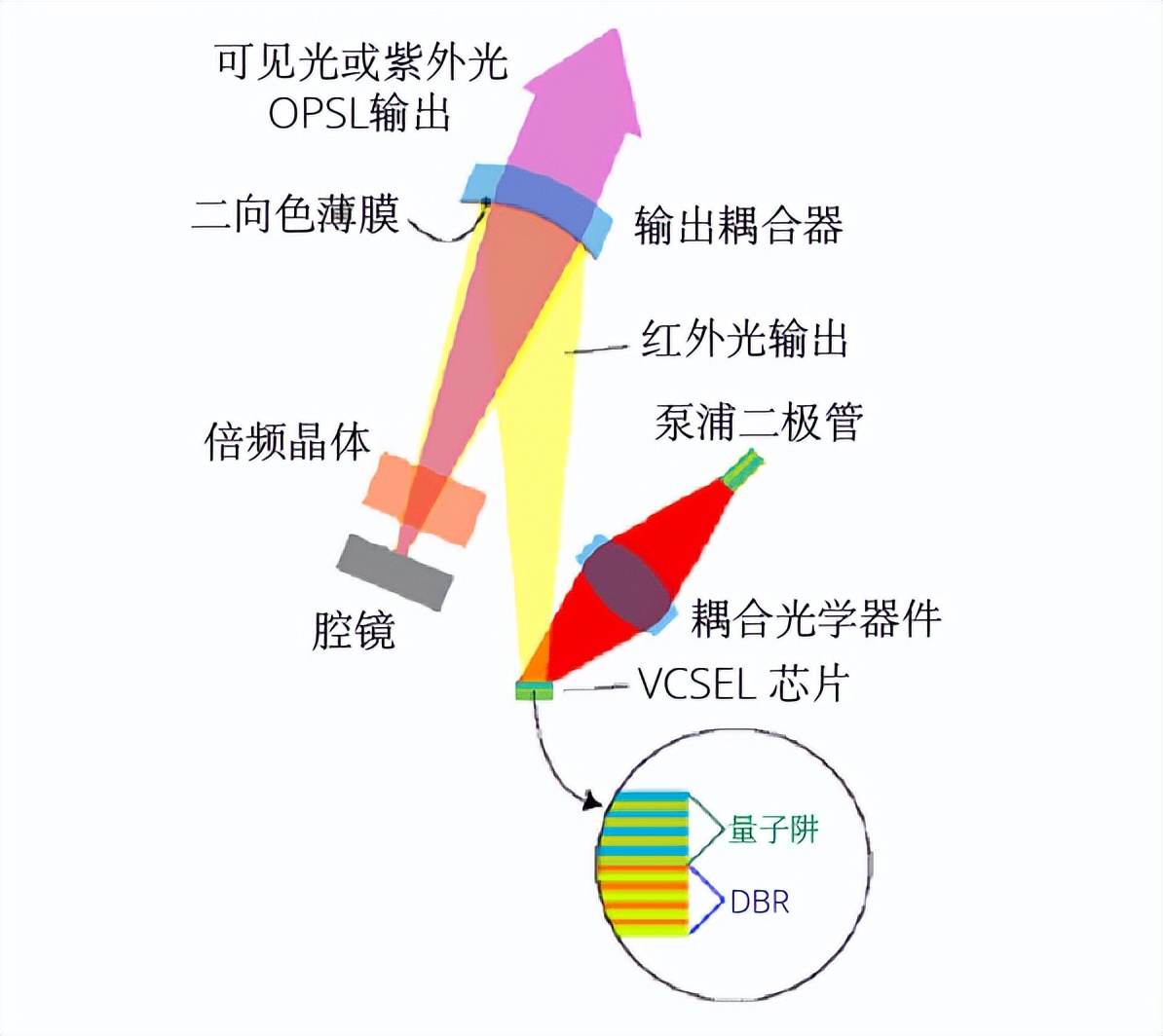
淺析推動生命科學發展的光泵半導體激光(OPSL)技術(三)
多波長激光引擎 - 生命科學儀器的未來
淺析推動生命科學發展的OPSL技術(二)

淺析推動生命科學發展的光泵半導體激光(OPSL)技術(一)




 生命科學領域下的醫藥研發應用了哪些技術
生命科學領域下的醫藥研發應用了哪些技術











評論