研究背景
鋰離子電池以其高能量密度、高轉換效率、長循環壽命等顯著特性,在電動汽車、航天飛行器、可變電子器件等領域得到了廣泛應用。與此同時,日益深入的應用場景也促使LIBs向著更高的能量密度和更長的壽命方向發展。而正極材料直接決定了鋰離子電池的性能。三元材料綜合了Ni、Co、Mn的優點,在正極材料中具有更大的潛力獲得比容量、功率密度、能量密度更高的電池。但隨著三元材料中鎳含量的增加和鈷含量的降低,LiNi0.8Co0.1Mn0.1O2(NCM 811)面臨著循環穩定性差、安全性降低的挑戰。為了解決這些問題,包覆方法被認為是一種很有前途的提高三元材料性能的技術。目前國內外對二氧化鈦包覆NCM材料的制備進行了一定研究,但仍未研究出一種操作簡單、成本低、更容易靈活控制NCM的粒度和形狀的方法。
成果簡介
近日,天津大學機械學院杜青教授教授研究了利用納米TiO2包LiNi0.8Co0.1Mn0.1O2制備出高電化學性能的三元鋰電池。通過采用草酸共沉淀法和無水乙醇濕包覆法制備了納米TiO2包覆NCM811正極材料,并研究不同包覆量下制備出的三元正極材料的性能。最終發現利用納米TiO2包覆方法可以減弱制備過程中的團聚現象和顆粒分散,從而提高氧化還原反應的可逆性,降低電池的阻抗和穩定的循環性能。并且,當納米TiO2包覆量為1.5%時,電池性能最佳,氧化還原峰差為0.083 V,第一次循環庫侖效率為95.98%。循環后,正極材料粒度過大會加速團聚現象,導致循環性能降低。這一工作有利于鋰電池的電極設計。此工作以“Fabricationof high electrochemical performance Ternary lithium battery using LiNi0.8Co0.1Mn0.1O2with nano-TiO2 coating ”為題,發表在Applied Energy 上。
研究亮點
1.采用草酸共沉淀法和濕法包覆法制備三元材料。
2.相對少量的納米TiO2包覆會減少陽離子混合現象。
3.表面包覆的方法會減弱NCM811材料的團聚現象。
4.適當的包覆量為1.5%,可獲得最佳電池性能。
5.循環后,包覆材料尺寸的增加是性能下降的主要原因。
圖文導讀
在這項工作中,作者提出了一種利用草酸共沉淀法和無水乙醇濕法包覆的方法制備出納米TiO2包覆NCM811正極材料。然后,研究了不同包覆量下制備的三元正極材料的性能。
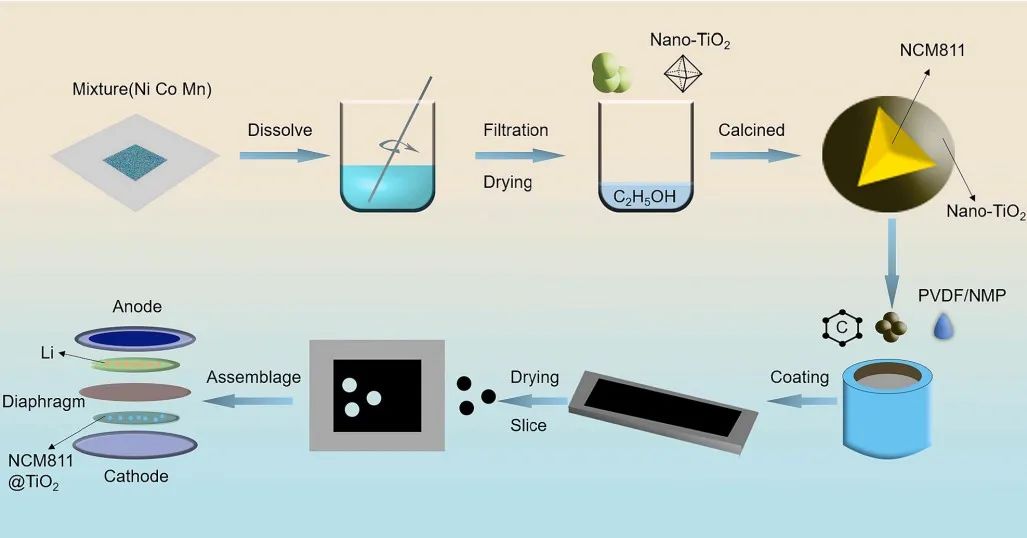
圖1. 包覆工藝和制備工藝。
首先,按照Ni: Co: Mn的摩爾比為81稱量醋酸鹽,然后將過量草酸固體混合在一起制備混合溶液,再將其進行離心過濾、干燥。為控制納米TiO2的包覆量,將不同質量比(質量比為0%、1%、1.5%、2.5%、4%)的納米TiO2與上述干粉混合,加入無水乙醇中進行濕法包覆,經干燥后,將得到的粉末顆粒分別用略微過量的鋰源Li2CO3在砂漿中充分研磨。為得到未包覆TiO2的NCM 811(Bare NCM 811)和包覆TiO2的NCM 811 (NCM 811@TiO2)的前驅體材料,將混合粉末分別轉移到馬弗爐,在450℃下預燒8 h,在800℃下高溫煅燒15 h。最后將制備好的Bare NCM 811和NCM 811@TiO2用于制備電池極片。
在制作極片之前,將粘結劑PVDF(聚偏氟乙烯)和N -甲基-2-吡啶酮(NMP)按1:32的質量比稱重,并在燒杯中攪拌至PVDF固體完全溶解于溶液中。然后,將正極前驅體材料(包括Bare NCM 811或NCM 811@TiO2)、導電炭黑和上述混合溶液中的粘結劑PVDF按81的質量比例混合,直至形成膏狀漿料。為保持電極材料的厚度,采用厚度為200 μm的刮板將混合漿料包覆在鋁箔表面。在真空干燥箱中80°C干燥后,可以從混合漿料中除去多余的NMP。然后,使用切片機將干燥的材料切割成直徑為12 mm的圓形片作為正極。負極采用直徑為12mm的鋰金屬薄片。這兩個電極由直徑為16 mm的celgard 2400膜分離,并在1.0 M LiPF6中浸泡在體積比為11Vol%的電解質中,分別為碳酸乙烯酯(EC)、碳酸二甲酯(DMC)和碳酸甲酯(EMC)。CR2032型紐扣電池安裝在氬氣手套箱中。

圖2. XRD掃描電鏡和透射電鏡圖像(a)NCM 811,Bare NCM 811, NCM 811@TiO2 的XRD圖譜(b)掃描電鏡模式Bare NCM811 (c)NCM 811@TiO2的掃描電鏡圖譜 (d)NCM 811@TiO2(NCM811@TiO2意味著NCM 811包覆二氧化鈦)的透射電鏡圖譜。
為了驗證包層后制備的NCM811材料的三元層狀結構,對合成材料進行了X射線衍射測試。圖2對比了商用NCM 811、Bare NCM 811和NCM 811@TiO2(本節中包覆TiO2的質量分數為1.0%)的X射線衍射(XRD)圖。結果表明,Bare NCM811呈現層狀α-NaFeO2結構,對應于R- 3 m空間基團。與商用NCM 811相比,NCM 811@TiO2的兩對分裂峰(106)/(102)和(108)/(110)更為明顯。這表明在NCM811@TiO2上包層不會改變NCM材料原有的層狀結構,將獲得高度有序的層狀結構。通過高鎳三元材料中I003/I104的比值可以判斷陽離子混合的程度。如圖2(a)所示,NCM 811@TiO2材料中I003/I104的比值大于其他兩種NCM材料,這意味著NCM811@TiO2的陽離子混合程度最弱,晶體結構最穩定。圖2(b和c)中的SEM圖像描繪了Bare NCM 811和NCM 811@TiO2的微觀形貌。納米TiO2的粒徑小于0.1 μm,比NCM 811的粒徑小。通常在制備過程中,(納米TiO2)的小顆粒會包裹在大顆粒(NCM811)的表面。如圖2b所示,未包覆的NCM811材料表面光滑。包層后,從圖2c可以看出,材料表面變得完全粗糙,顆粒尺寸增大。它呈現出光滑與粗糙交替的現象。Bare NCM 811顆粒是由小塊狀顆粒聚集形成的,其形狀不規則。相比之下,NCM 811@TiO2顆粒具有分散性好、尺寸均勻、形貌與單晶三元材料相似的優點。在Bare NCM811中,顆粒聚集形成球形度較差的二次顆粒。然而,NCM 811@TiO2顆粒表面比原始材料更粗糙。粗糙的表面會抑制正極材料與電解液的反應,減少副反應引起的正極活性物質的溶解。與Bare 的NCM 811相比,包層后NCM 811@TiO2顆粒的比表面積增大,因為顆粒更加分散,有利于Li+在電極表面的脫嵌。為了證明納米TiO2包層在正極材料表面的存在,對NCM 811@TiO2顆粒進行了TEM成像。如圖2d所示,TiO2納米顆粒成功地包覆在NCM811大顆粒表面,形成保護層。
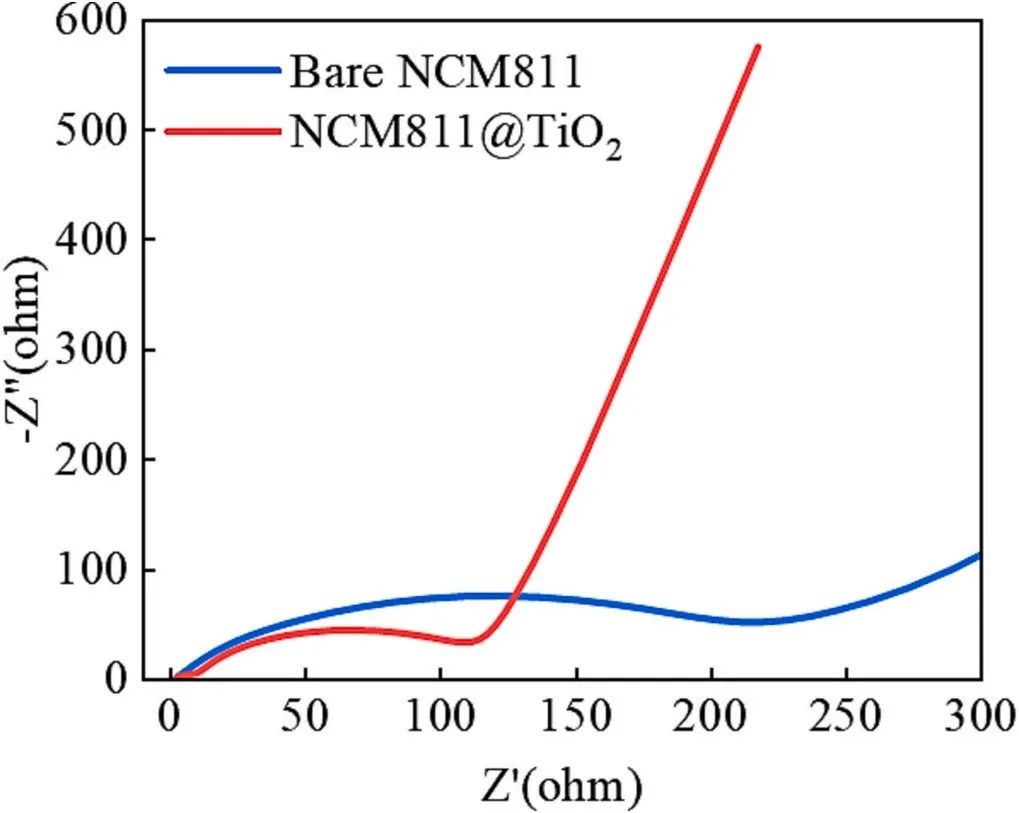
圖3. Bare NCM811和NCM的EIS分析811@TiO2。
通過EIS分析,對Bare NCM 811和NCM 811@TiO2的電化學阻抗進行分析(圖3)。雖然NCM 811@TiO2的歐姆阻抗與BareNCM 811幾乎相同,但其極化阻抗僅為Bare NCM 811的一半。這意味著覆膜電極材料對Li+的脫嵌阻力更低,離子更容易擴散,這將增強電極材料的循環性能。
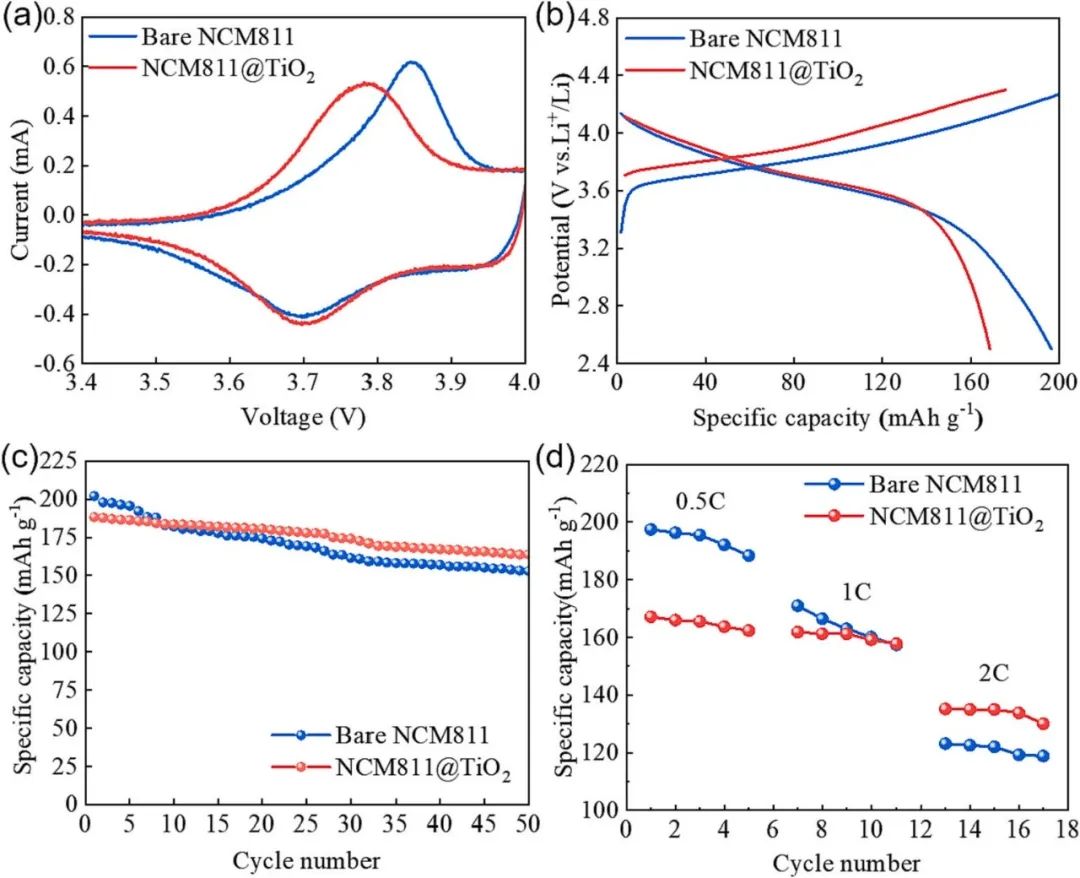
圖4. Bare NCM 811和NCM 811@TiO2 (a)循環伏安圖(b)第一循環庫侖效率在0.5C(c) 50循環炭放電圖在0.5C (d)速率性能圖在0.5C,1C,2C。
之后,循環伏安法和充放電試驗如圖3所示。從圖4(a)的循環伏安圖來看,Bare NCM811和NCM 811@TiO2的還原峰基本一致(約3.7 V),但NCM 811@TiO2的氧化峰更接近還原峰。Bare NCM811的氧化還原峰差為0.146 V,而NCM 811@TiO2的氧化還原峰差為0.104V,說明NCM 811@TiO2材料在氧化還原反應(ORRs)中具有更好的循環可逆性。因此,包層過程會降低陽離子的混合程度和Li+與Ni2+之間的占據現象,從而使更多的Li+參與反應,提高NCM 811@TiO2電池的循環性能。圖4(b)為兩種材料在0.5C時的比容電壓圖。第一循環庫侖效率是第一次放電的比容量與第二次充電的比容量之比。顯然,NCM 811@TiO2的放電比容量(161.3mAh?g?1)低于Bare NCM 811的放電比容量(196.3 mAh?g?1),說明NCM 811@TiO2的整體比容量更小。其主要原因是表面包覆的納米TiO2會占據活性位置,使參與反應的活性物質減少。但NCM 811@TiO2的第一循環庫侖效率(95.98%)高于Bare NCM 811的95.46%。對于高鎳低鈷三元材料,隨著材料中鎳含量的增加,第一次循環的庫侖效率會逐漸降低。由此可見,庫侖效率的提高證明了納米TiO2包層可以提高電化學循環性能,更有利于電池的循環壽命。
為了進一步探索材料的循環性能和放大性能,在圖4 (c和d)中進行了0.5C條件下的50次循環試驗和三種不同放電速率下的倍率試驗。電池循環50次后,Bare NCM 811的容量衰減率為23.44%,大于NCM 811@TiO2的22.60%。這意味著包層方法將改善循環性能和容量保持。
此外,NCM 811@TiO2在不同放電速率下的穩定性較好。然而,在不同的放大倍數下,比容量下降,因為包層材料的顆粒更分散,不會聚集成大顆粒。而NCM 811@TiO2材料的結構會縮短鋰離子的擴散路徑,使更多的鋰離子擴散到電解質中,循環性能更穩定。不幸的是,電池的比容量仍然在減少。
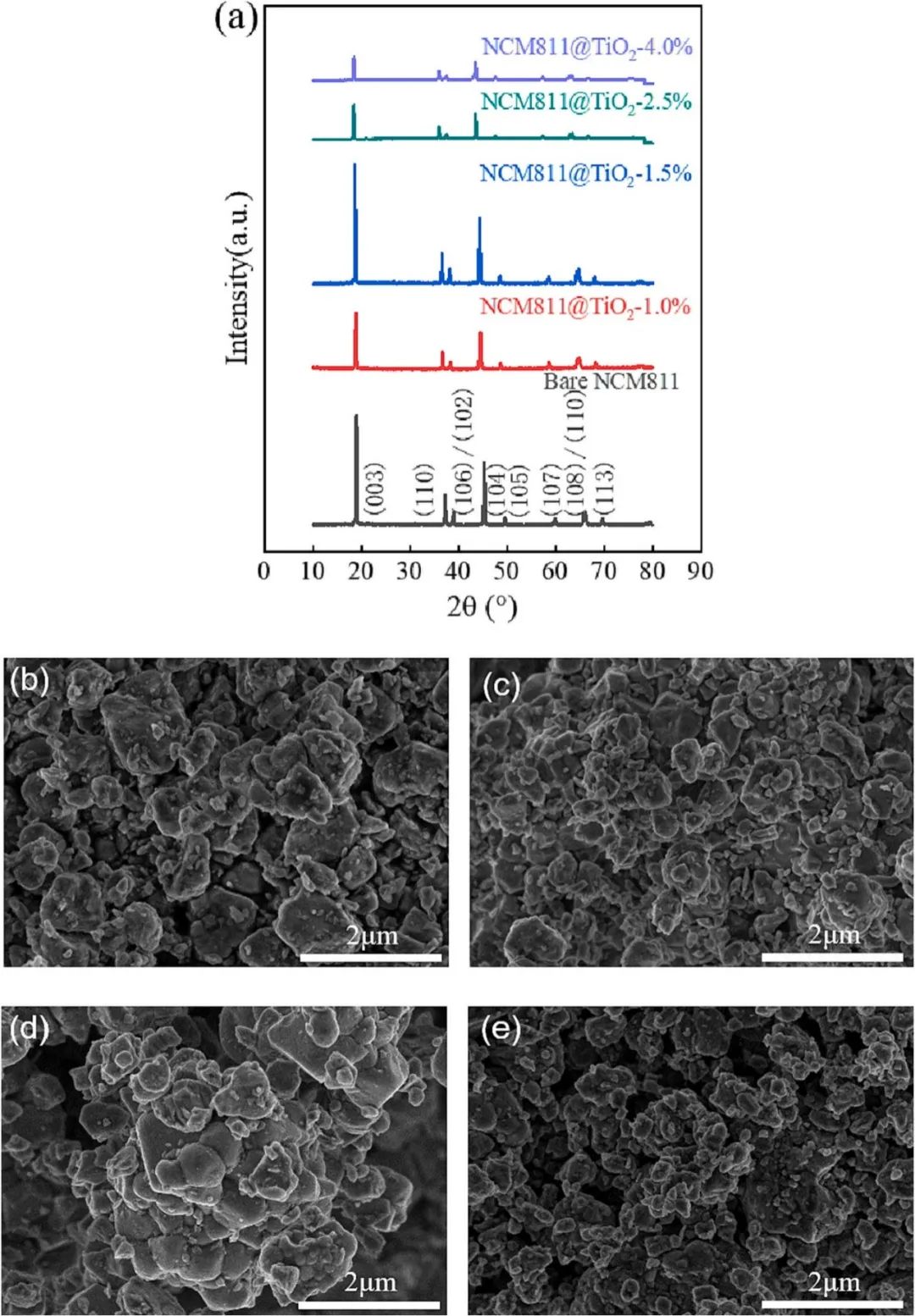
圖5. XRD和SEM圖像(a) Bare NCM 811,NCM811@TiO2–1.0%,NCM 811@TiO2–1.5%,NCM811@TiO2–2.5%,NCM 811@TiO2–4.0%的XRD圖譜;(b-e)NCM811@TiO2–1.0%、NCM 811@TiO2–1.5%、)NCM811@TiO2–2.5%、NCM 811@TiO2–4.0%.的掃描電鏡圖譜(NCM811@TiO2–1.0%表示NCM 811包層1.0%二氧化鈦)。
表1不同材料的I003/I104值
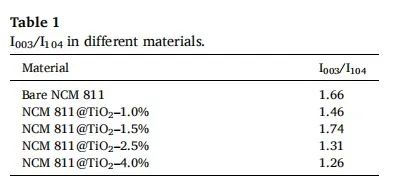
為了獲得更好的電池性能,制備了不同納米TiO2包覆量的NCM 811@TiO2,并采用XRD和SEM方法分析了其微觀形貌和晶體結構。圖5(a)為不同納米TiO2包覆量對應材料的XRD。從圖5(a)中可以看出,不同包覆量的材料呈現出相同的X射線光譜,說明所有材料都具有α-NaFeO2和R-3 m空間基團的層狀結構。這也意味著包覆量不會影響NCM 811@TiO2材料的層狀結構和相結構。不同包覆量的材料對應的I003/I104的比值如表1所示。可以看出,NCM811包層1.5% TiO2 (NCM 811@TiO2-1.5%)材料的陽離子混合度最低(I003/I104 = 1.74),說明相對少量的納米TiO2包層可以減少陽離子混合現象,對電池性能影響較弱。但隨著包布量的進一步增加,陽離子混合現象更加嚴重,包布4% TiO2 (NCM 811@TiO2 -4%) (I003/I104 = 1.26)的NCM 811中I003/I104的比例甚至遠低于Bare NCM 811 (I003/I104 = 1.66)。這主要是由于顆粒的聚集導致鋰離子擴散量的減少,導致Li+和Ni2+混合更嚴重。
圖5(b-e)為不同包覆量的NCM 811@TiO2材料對應的微觀結構。所有這些具有不同包層量的材料在其表面形成粗糙的保護層。相比之下,小的包覆量將產生材料顆粒的高分散性和活性物質與電解質之間的大接觸面積,從而提高電極材料的穩定性和循環性能。然而,過量的包覆量會在初次團聚現象減弱后導致二次團聚。二次團聚會降低材料的微觀比表面積,導致材料與電解質之間的有效接觸面積變小。顆粒團聚會使Li+的擴散路徑發生較大變化,從而影響材料的整體性能。
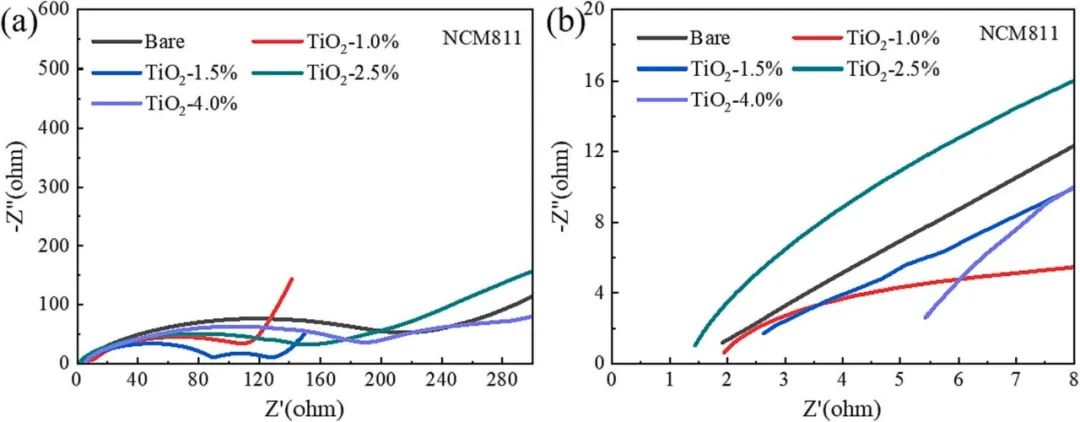
圖6. (a)Bare NCM 811,NCM811@TiO2–1.0%,NCM 811@TiO2–1.5%,NCM811@TiO2–2.5%,NCM 811@TiO2–4.0%的電化學阻抗譜。(b)阻抗的局部放大率為0-8Ω。
不同包覆量材料的電化學阻抗對比如圖6所示。交點之間的高頻率區和實軸的阻抗為歐姆阻抗。在高頻區與半圓相對應的半徑表示電池的電荷轉移阻抗。低頻區Warburg尾的傾斜程度反映了Li+的擴散阻抗。從圖6(a)可以看出,隨著包層量的增加,極化阻抗呈現先減小后增大的趨勢。從圖6(b)可以看出,NCM 811包層2.5% TiO2 (NCM 811@TiO2-2.5%)的歐姆阻抗最小。相比之下,極化阻抗的變化更為顯著。NCM 811@TiO2 -1.5%的極化阻抗最小。主要原因是在少量的納米TiO2包層下,顆粒的團聚被削弱,更加分散。因此,NCM 811@TiO2 -1.5%具有導電性,擴大了活性材料之間的接觸面積,可以使反應更充分,增強Li+的脫插。
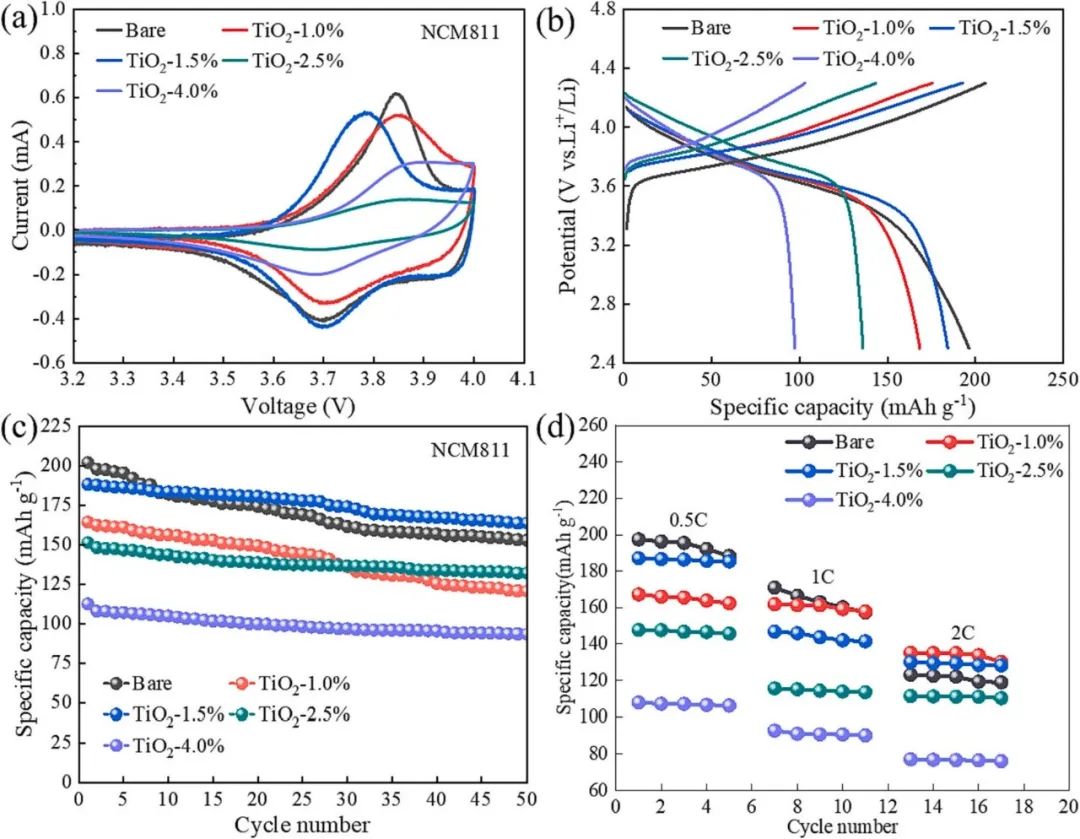
圖7. Bare NCM 811,NCM 811@TiO2–1.0%,NCM 811@TiO2–1.5%,NCM 811@TiO2–2.5%,NCM 811@TiO2–4.0%(a)循環伏安圖(b)第一循環庫侖效率在0.5C (c) 50循環充放電圖在0.5C (d)速率圖在0.5C,1C,2C的性能圖。
表2不同材料的氧化還原峰差值

表3不同材料的第一次循環的庫倫效率
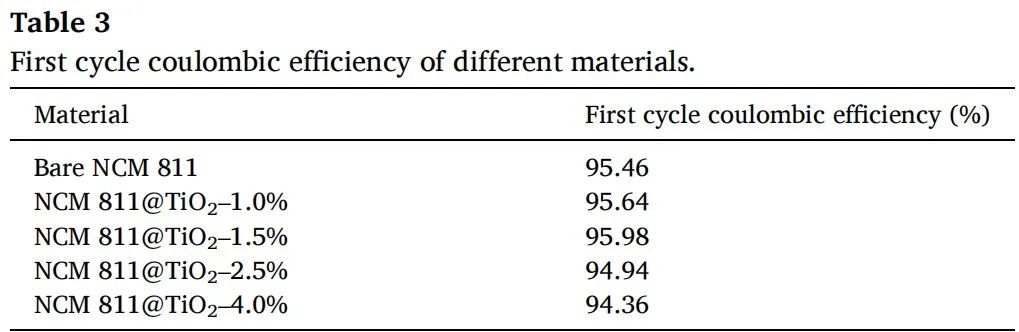
圖7(a)為不同材料包覆量電池的重復循環伏安測試曲線圖。可以看出,所有材料的還原峰都比較接近,在3.69 V左右。氧化峰明顯抵消。表2給出了所有材料對應的氧化峰和還原峰的差值。NCM 811@TiO2 -1.5%氧化還原峰差最小(0.083V),具有最好的可逆性。主要原因是少量包覆后活性物質與電解質之間的副反應會減少,活性物質的溶解也會減少,從而逐漸提高氧化還原反應的可逆性。NCM 811@TiO2 -1.5%顆粒分散性好,反應比表面積增大,更有利于Li+的提取和插入。但如果包布量過大,則會使整體可逆性變差。圖7(b)為0.5C時不同材料包覆量電池的容量-電壓比效圖。在比容量方面,所有包層材料的初始放電比容量均低于Bare NCM 811。表3為放電速率為0.5C時,不同包覆量材料對應的第一循環庫侖效率。可以看出,少量包覆后,第一個循環庫侖效率略有提高。然而,隨著包層量的增加,第一次循環的庫侖效率呈明顯的下降趨勢。圖7(c和d)為0.5C時的50循環性能圖和0.5C、1C和2C時的速率性能圖。從這兩張圖可以看出,電池的整體比容量隨著包層量的增加而減小。但在循環性能方面,隨著包層量的增加,電池材料的容量衰減變得更加平滑,說明增加包層量確實可以提高材料的容量保持率。其主要原因集中在以下兩個方面:一方面,包覆量大會增加包覆層厚度,使參與反應的Li+數量減少,影響整體充放電性能。另一方面,隨著包覆量的增加,相同質量的電極材料中活性物質的比例會變小,可提取插層的Li+總量減少,導致電池比容量逐漸下降。

圖8.(a-d)NCM 811@TiO2–1.0%、NCM 811@TiO2–1.5%、NCM 811@TiO2–2.5%、NCM 811@TiO2–4.0%的50個周期后的掃描電鏡圖譜。
圖8為拆卸電池經過50次循環充放電后正極片的SEM圖像。經過50次循環后,四種材料的粒徑均比原始粒徑大。顆粒表面會形成一層SEI膜,導致電池性能下降。少量包覆后,團聚效果不是很明顯(圖8a)。當包覆量為0.03 g時,結塊現象基本消失。循環50次后,在NCM 811@TiO2 -1.5%的SEM圖中未發現二次團聚現象和較大的顆粒(圖8b),說明循環穩定性較好。但隨著包覆量的增加,二次團聚現象更加明顯(圖8c和圖8d),團聚顆粒在其表面附著的沉積物更多,形成體積顆粒更大,循環性能較差。因此,NCM 811@TiO2 -1.5%的正極三元材料表現出最好的性能。
總結與展望
本文作者通過材料表征和電化學分析實驗,探討了納米Tio2包覆高鎳三元材料對正極材料微觀結構和電化學性能的影響因素。發現包覆后的NCM 811材料顆粒更加分散,提高了電池的循環性能和放大性能。相對少量的納米TiO2包覆可以減少Ni+離子引起的陽離子混合現象,對電池性能的影響較弱。包覆量為1.5%的三元材料呈現顆粒均勻分散和弱團聚現象,使其在第一次循環時達到最佳的循環穩定性和最高的庫侖效率。然而,隨著包覆量的進一步增加,會發生二次團聚,導致比表面積降低,陽離子混合嚴重。在循環試驗中,我們發現循環后正極材料顆粒直徑的增大是導致性能下降的主要原因。循環后,包覆量為1.5%的材料仍保持分散狀態,無明顯結塊現象,可減少正極活性物質與電解質副反應引起的活性物質溶解,提高循環穩定性。這些結論可為正極材料的設計和鋰電池性能的改善提供有意義的實驗建議。
文獻鏈接
An, L., W. Li, J. Wang,et al. “Fabricationof high electrochemical performance ternary lithium battery using LiNi0.8Co0.1Mn0.1O2with nano-TiO2 coating.” AppliedEnergy 355: 122272.
DOI:10.1016/j.apenergy.2023.122272.
-
正極材料
+關注
關注
4文章
326瀏覽量
19222 -
TiO2
+關注
關注
0文章
4瀏覽量
8104 -
三元鋰電池
+關注
關注
8文章
182瀏覽量
15866
原文標題:天津大學杜青Applied Energy:利用納米TiO2包覆LiNi0.8Co0.1Mn0.1O2制備高電化學性能的三元鋰電池
文章出處:【微信號:清新電源,微信公眾號:清新電源】歡迎添加關注!文章轉載請注明出處。
發布評論請先 登錄
相關推薦
具有優越循環性的雙重改性的低應變富鎳正極軟包全電池




















評論