細胞重編程技術可用于獲得或研究臨床所需的目的細胞類型,在再生醫(yī)學、疾病模型構建和藥物篩選中具有廣泛的應用。相較于經(jīng)典的多潛能干細胞(iPSCs)重編程技術,直接重編程通過規(guī)避干細胞耗時的分化過程,能夠直接將一種成體細胞轉化為另一種所需的功能細胞類型,例如將成纖維細胞轉化為誘導神經(jīng)元(iN)細胞。然而,這些轉換過程的低效率為生物醫(yī)學應用帶來了障礙。細胞直接重編程的一個關鍵步驟是克服異染色質(zhì)的表觀遺傳屏障并打開內(nèi)源基因進行細胞類型轉換。
過往研究主要集中在轉錄因子和生化因子在細胞表型轉換中的作用,但對生物物理因子的影響知之甚少。細胞在不同時間尺度上(從幾秒到幾天)經(jīng)歷機械刺激,可能啟動力化學信號傳導、細胞骨架重組和染色質(zhì)重構。
據(jù)麥姆斯咨詢報道,近期,加州大學洛杉磯分校生物工程系李松教授課題組(第一作者為宋陽)在Nature Materials期刊發(fā)表了題為“Transient nuclear deformation primes epigenetic state and promotes cell reprogramming”的研究論文。該研究報道了懸浮細胞在通過一個狹窄的微流控通道時細胞核會經(jīng)歷一次快速的擠壓,這一可逆的細胞核形變過程可以顯著降低組蛋白H3K9和DNA的甲基化水平,繼而提高染色質(zhì)可及性,最終促進成纖維細胞向神經(jīng)元細胞的重編程效率。
為了直接確定核變形對染色質(zhì)重塑的影響,研究人員研究了通過擠壓懸浮細胞是否以及如何調(diào)節(jié)表觀遺傳狀態(tài)和細胞重編程,并探索了這種力學刺激方式向工業(yè)運用轉化的可行性方案。
在這項研究中,李松教授團隊通過微制造技術構建了一套具有寬度為7μm的微通道陣列的微流控器件,并讓轉染了神經(jīng)元相關轉錄因子(Brn2、Ascl1、Mytl1)的懸浮成纖維細胞在20μL/min的流速下通過微通道。研究發(fā)現(xiàn),細胞核受到擠壓的成纖維細胞其向神經(jīng)元細胞直接重編程的效率與對照組相比提高了8倍。
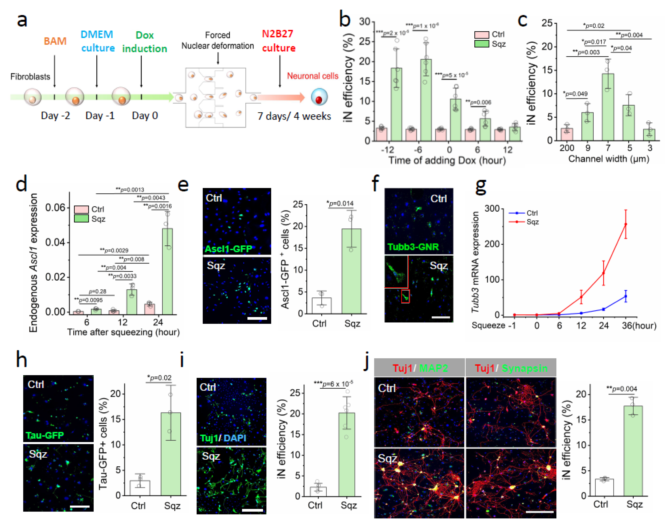
圖1 細胞核受到擠壓后,直接重編程效率顯著升高
通過對細胞表觀遺傳狀態(tài)的探索發(fā)現(xiàn),細胞受到瞬時擠壓后的24小時內(nèi),組蛋白H3K9和DNA的甲基化水平均顯著性下降。同時,力學誘導的H3K9me3和5m-C下降與通過抑制劑聯(lián)合處理細胞24小時后的下降水平基本一致。此外,通過與加州大學圣地亞哥分校(UCSD)王英曉教授合作,借助活細胞FRET技術實時觀測H3K9me3水平發(fā)現(xiàn),在成纖維細胞進入微通道1分鐘內(nèi),H3K9me3水平下降顯著。
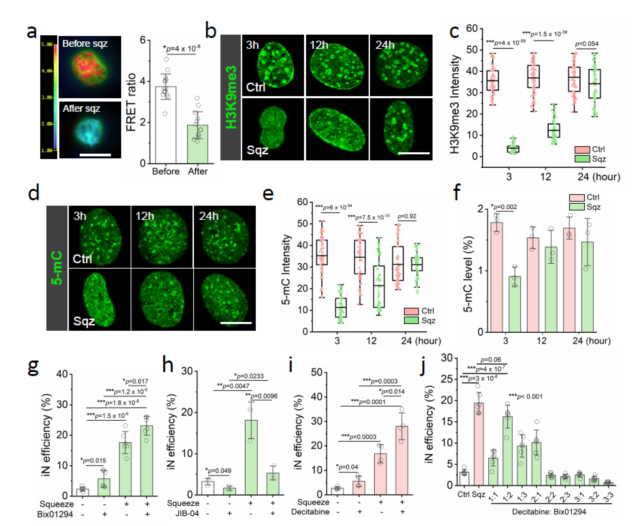
圖2 細胞核受擠壓后組蛋白H3K9和DNA甲基化降低
為進一步推進上述微流控器件的實際應用,李松教授團隊設計了一款高通量的微流控芯片,其在短時間內(nèi)可以實現(xiàn)百萬數(shù)量級細胞的力學刺激。此外,這一微流控器件不僅可以促進成纖維細胞向神經(jīng)元細胞重編程,也可以并不限于促進成纖維細胞向多潛能干細胞(iPSCs)重編程,以及巨噬細胞向神經(jīng)元細胞重編程。
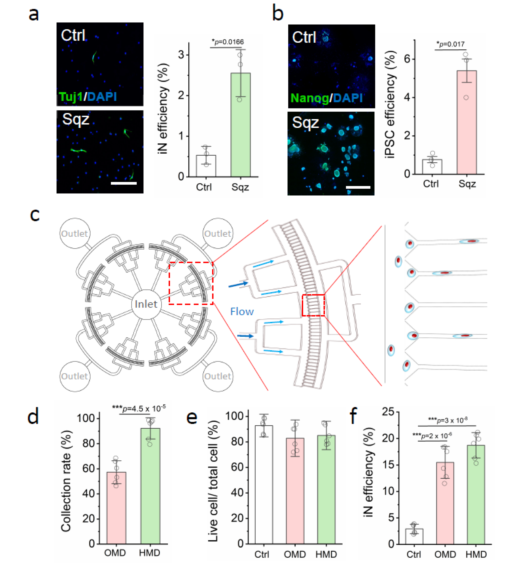
圖3 高通量芯片設計以及多種類型重編程實踐
該研究揭示了細胞核的力學變形會影響染色質(zhì)組織形式并誘導更開放的染色質(zhì)結構,可以廣泛運用于基因編輯領域。
-
編程技術
+關注
關注
0文章
40瀏覽量
10525 -
微流控芯片
+關注
關注
13文章
292瀏覽量
19066
原文標題:基于微流控的細胞核擠壓刺激變形,促進細胞重編程
文章出處:【微信號:Micro-Fluidics,微信公眾號:微流控】歡迎添加關注!文章轉載請注明出處。
發(fā)布評論請先 登錄
相關推薦
嵌入式軟件開發(fā)中常用的狀態(tài)機編程實現(xiàn)
基于改進遺傳算法的圖像分割方法
DNA甲基化與表觀遺傳學數(shù)據(jù)挖掘與分析學習會 (10月26-27 上海) 精選資料分享
遺傳算法的特點和應用概述
離體培養(yǎng)下的遺傳與變異
混沌遺傳算法優(yōu)化管網(wǎng)狀態(tài)神經(jīng)網(wǎng)絡模型
基于ARM7的重介參數(shù)自動調(diào)節(jié)系統(tǒng)

研發(fā)遙控免疫療法 可辨識和殺死癌細胞
微流體重編程以實現(xiàn)人誘導多能干細胞的多能性
基于光遺傳工程化活細胞的類生命光電晶體管
mTORC1高活性的干細胞樣狀態(tài)腫瘤細胞類型分析
光遺傳學 – 用光控制細胞和動物



















評論