活細胞的粘彈性力學性質與人類疾病的進程息息相關,肌動蛋白細胞骨架(F-actin)是細胞骨架系統的重要組成部分,在控制細胞結構、運動和傳感方面具有重要意義,尤其是細胞骨架的重新排列會導致力學性質的顯著變化。因此,對于細胞骨架結構形貌、粘彈性力學性質的原位表征格外重要。然而,迄今為止,已有研究方法無論是光學手段還是牽引力顯微鏡、納米壓痕等力學手段都缺乏在液相環境下對活細胞的細胞骨架結構和力學性質的原位表征。
為了這一實驗目的,中山大學物理學院物理力學與生物物理研究中心團隊通過改進并發展了可在液相下原位測量活細胞的多頻率調制原子力顯微鏡技術(AM-FM AFM)。對原有的只能在大氣環境下工作的AM-FM設備進行改進,將懸臂完全浸沒在液相環境中。
利用細胞培養基的阻尼,代替原來不能在液體中使用的阻尼材料,消除偏離原子力顯微鏡標準共振的其他介質的擾動, 懸臂振蕩的高效穩定性能夠提高測量信噪比。此外,通過實驗修正液相下懸臂的二階頻率漂移,定量獲得細胞合理的力學性質。在原位微環境下實現了細胞骨架結構形貌、粘彈性的同時成像,分辨率達到50nm。
此外,對于癌細胞而言,腫瘤組織微環境不斷酸化,癌組織中細胞外的pH值(~6.5)低于正常組織的基本值(~7.4)。在癌癥等多種疾病的研究中發現,酸性微環境促進癌細胞的遷移進程從而引起侵襲,這一過程與偽足結構(由F-actin構成)的改變有關。
然而,在不同的pH微環境下,細胞骨架組織、粘彈性特性和細胞遷移之間的相關性仍然知之甚少。這篇文章通過改進的AM-FM AFM,觀察到正常環境下,癌細胞偽足中的細胞骨架呈短小、松散分布,相應的彈性和粘性沿偽足延伸方向近乎水平。
而酸化環境下,癌細胞偽足中的F-actin聚合并編織成一個長而粗的束狀結構,指向偽足前端的延伸方向,相應的彈性和粘性沿著該方向均呈現明顯的梯度增加。粘性和彈性的增加有利于癌細胞偽足前端的粘附,使細胞在收縮過程中,前端牢牢地粘附基底,并有足夠的剛性提供向前的驅動力,利于細胞遷移過程。實驗結果說明酸性環境下通過改變細胞骨架的構象,使偽足前端的彈性和粘性梯度增加,從而促進癌細胞的粘附和遷移的機制。
該研究結果對于理解細胞骨架F-actin和粘彈性在改變細胞形態和行為方面的意義具有重要指導作用,并為在pH微環境下癌細胞轉移開辟了一個新的納米力學機制模式。此外,該方法實現細胞骨架在液相下結構和粘彈性力學性質的同時表征,并達到50nm的分辨率,為推進不同微環境包括不同氧氣濃度、不同離子溶液等模擬不同種類細胞的生理環境研究邁出重要的一步,從微觀結構探索細胞的自適應過程,為理解細胞骨架調節細胞的功能命運提供方法依據。
該成果以“Effect of F-actin organization in lamellipodium on viscoelasticity and migration of Huh7 cells under pH microenvironment using AM-FM atomic force microscopy”為題發表在Frontiers in Physics期刊上(doi: 10.3389/fphy.2021.674958),中山大學物理學院研究生陳苗為第一作者,朱文鵬教授和張瀟悅副教授為共同通訊作者。研究工作得到了國家自然科學基金面上項目、國家重大科研儀器研制項目以及廣東省自然科學基金的支持。
編輯:jq
-
力學
+關注
關注
1文章
51瀏覽量
15321 -
原子
+關注
關注
0文章
89瀏覽量
20492
原文標題:原子力顯微鏡案例分享: AM-FM液相下原位成像細胞骨架的結構和粘彈性分布
文章出處:【微信號:zhishexueshuquan,微信公眾號:知社學術圈】歡迎添加關注!文章轉載請注明出處。
發布評論請先 登錄
相關推薦
功率放大器在液滴微流控細胞分選中的應用

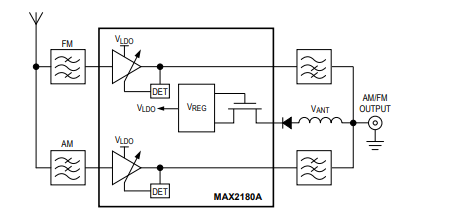
MAX2180A AM/FM汽車天線低噪聲放大器技術手冊
車身骨架焊接技術解析與應用

應用于活細胞成像的一次性細胞培養芯片
基于玻璃基底的細胞培養芯片研究(下)
靜態與動態載荷下具有粘彈性密封劑光伏組件的力學特性分析

阻尼器的工作原理及機制解析
不同材質的阻尼器性能比較
活細胞的“聚光燈”——前沿活細胞成像的案例分享



















評論